Laser et P-D-T (Photothérapie Dynamique) sans colorant : Une alternative de soins
 Les techniques de décontamination lasers assistées sont intégralement reprises dans leur historique, dans les possibilités d'actualité en Parodontologie, en Endodontie et en Implantologie, mais également dans les recherches en cours qui touchent de nombreux domaines médicaux.
Les techniques de décontamination lasers assistées sont intégralement reprises dans leur historique, dans les possibilités d'actualité en Parodontologie, en Endodontie et en Implantologie, mais également dans les recherches en cours qui touchent de nombreux domaines médicaux.
par le Dr Gérard Rey, Parution LS 76, novembre 2017
Résumé :
Après avoir indiqué l'historique des études scientifiques et cliniques qui ont abouti à la découverte d'une méthode de décontamination efficace dénommée "Photothérapie dynamique sans colorant", l'auteur montre l'intérêt d'un partenariat entre les équipes scientifiques et l'industrie Européenne pour améliorer le matériel médical et rendre les traitements plus simples et plus performants.
Des démonstrations de cas cliniques témoignent des résultats exceptionnels en Parodontologie, en Endodontie, en Implantologie ainsi qu'en Chirurgie et en Médecine.
La dernière partie est consacrée aux recherches en cours et au long travail restant à faire pour améliorer la santé publique par une prévention mieux comprise qui doit permettre une orientation vers une "Médecine dentaire" de qualité et accessible, avec l'objectif de maintenir la sphère bucco-dentaire dans son état naturel le plus longtemps possible.
LASERS ET P.D.T. SANS COLORANT : UNE ALTERNATIVE DE SOINS ET DE PREVENTION D’INTÉRÊT COLLECTIF
INTRODUCTION
A. Les constats en matière de prévention
B. Les constats en matière de Sécurité
C. Historique et Premières recherches sur les Lasers médicaux
D. Etudes des propriétés des Lasers médicaux
E. Découverte de la PDT sans colorant
F. Vérification in vitro en laboratoire
G. Les constatations cliniques in vivo
H. Les problèmes techniques liés à la maitrise des effets thermiques
I.La solution : Partenariat Scientifiques / Industriels et naissance de la technologie actuelle
J. Les Applications en Médecine Dentaire
- En Parodontologie
- En Endodontie
- En Dentisterie
K. Les Applications cliniques en Odontostomatologie
L. En Implantologie
M. En Stomatologie
N. Les Applications en Médecine
-
Les plaies post chirurgicales
-
Les escarres
-
Les infections bactériennes
O. Quelques recherches complémentaires
-
Recherches universitaires sur la Biostimulation
-
PDT sans colorant et CNRS de Lille
-
Recherche sur l’Oxygéno-thérapie à l’Université KU Leuven
P. Un long travail reste à faire
-
Un travail scientifique de laboratoire et un travail technique industriel
-
Un travail d’Enseignement et de Formation
-
Un travail de Prévention et de Santé Publique
-
Parlons économies
Conclusions
Lire aussi sur les lasers :
La maintenance parodontale : acte essentiel aprés traitement des parodontites et peri implantites
Regénération osseuse assistée par laser
Simplicité et efficacité en hygiène bucco-dentaire
Place des lasers en Esthétique bucco dentaire quotidienne
Influence de l’utilisation d’un laser diode dans l’extraction des dents de sagesse incluses
Avulsion d'une racine fracturée en vue d'implantation assistée par laser
INTRODUCTION
Après avoir décrit l’historique des recherches d’actualité dans les nouvelles technologies impliquant les lasers médicaux, nous ferons un inventaire des applications possibles en Chirurgie dentaire, en Stomatologie et en Médecine.
Les recherches universitaires actuelles permettent d’espérer de réelles améliorations en matière de santé générale qui pourraient être accompagnées d’un remodelage du « Business Modèle » de l’assurance de santé afin de permettre une évolution professionnelle axée vers la Prévention et « la conservation le plus longtemps possible de la sphère endo-buccale dans son état naturel » (CNO 2015).
La bonne santé générale est, pour une partie importante, fonction de la bonne santé bucco-dentaire et parodontale. La Prévention est donc un axe de réflexion prioritaire qu’il convient de prendre en considération avant toute décision concernant la santé. (Fig. 1)

Fig. 1. La Prévention : une obligation professionnelle d’intérêt collectif
A. LES CONSTATS EN MATIÈRE DE PREVENTION
La prévention est une « habitude de vie » qui concerne notre travail, nos activités de loisirs et notre nourriture. Elle permet d’éviter une chute des défenses immunitaires qui s’accompagnent souvent d’une chute des défenses psychiques (RIOU J et al 2013).
Au niveau bucco-dentaire, la prévention peut permettre de vivre une vie d’adulte et de sénior en évitant les dépenses très importantes des reconstructions prothétiques. Les avantages sont esthétiques, fonctionnels et financiers (Fig. 2) :
-
Conserver la séduction d’un sourire naturel que nulle prothèse ne saurait remplacer
-
Préserver la solidité de notre système masticatoire qui permet une bonne assimilation alimentaire
-
Eviter le désagrément des longues séances de réhabilitation orale, parfois accompagnées de devis très importants (souvent tout à fait justifiés).

Fig. 2- La prévention permet aux adultes et aux séniors d’éviter les dépenses importantes des reconstructions prothétiques
La conservation d’une bonne et belle dentition dépend de 3 facteurs :
-
Le rôle essentiel du patient qui intervient pour 50 % du résultat, particulièrement grâce à l’hygiène bucco-dentaire quotidienne.
-
Le statut médical du patient qui intervient pour 25 %. Critère sur lequel il est possible d’intervenir en dominant les facteurs aggravants (tabagisme, alcoolisme, …) et en conservant une activité physique et intellectuelle pendant toute sa vie.
-
Le praticien médecin ou chirurgien-dentiste intervient pour environ 25 %, mais a sous sa responsabilité l’intégralité des soins médicaux et des réfections prothétiques dont le choix des traitements et la qualité des soins effectués impactent fortement la maintenance et la prévention future.
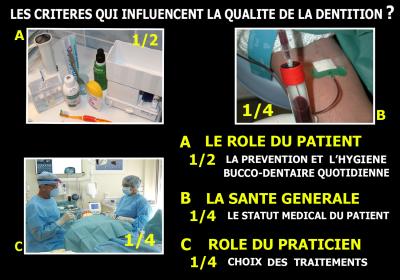
Fig. 3 - En santé bucco-dentaire comme en santé générale, le rôle du patient est essentiel
B. LES CONSTATS EN MATIÈRE DE DEPENSES DE SANTÉ
Les dépenses en matière de soins dentaires, de chirurgie implantaire ou de prothèses bucco-dentaires sont une charge très importante, à la fois pour la partie qui reste en charge pour les ménages (Fig. 4) et également pour la partie financée par les organismes complémentaires (Fig. 5).

Fig. 4 - Statistiques de la Direction de la Recherche, des Etudes, de l’Evaluation et des Statistiques (D.R.E.E.S)
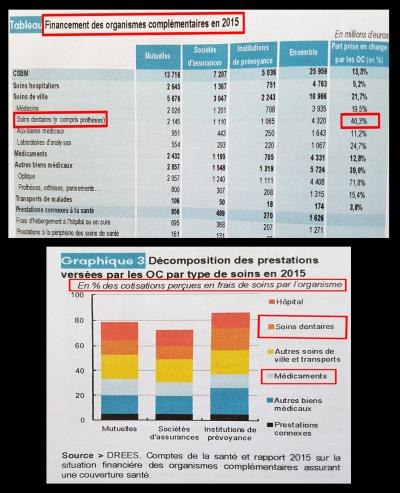
Fig. 5.
Les postes de consommation des soins et biens médicaux (C.S.B.M.) restent de manière importante à la charge des ménages, particulièrement en ce qui concerne les soins de ville et les médicaments.
Le poste « soins dentaires » restant à la charge des patients est en pourcentage le plus important avec le poste optique.
En ce qui concerne le financement par les organismes complémentaires, le constat est tout aussi alarmant.
La prise en charge des soins dentaires et des prothèses représente une part extrêmement importante dans le financement des organismes complémentaires. (L’état de santé de la population en France – Rapport 2017 Ministère des Solidarités et de la Santé).

Fig. 5 - Financement par les organismes complémentaires – (Origine D.R.E.E.S.)
Il est évident qu’une prévention améliorée peut amener un allègement de ces dépenses de santé.
C. HISTORIQUE ET PREMIERES RECHERCHES SUR LES LASERS MÉDICAUX
La Parodontologie, qui s’intéresse aux tissus de soutien osseux et gingivaux, est la base de la prévention qui permet de conserver l’écosystème bucco-dentaire dans son état naturel. Malheureusement, de nombreux adultes sont victimes du manque de prévention et les maladies parodontales sont extrêmement nombreuses particulièrement chez les adultes après 45 ans. (Charron J, Mouton C. 2003). La pratique en milieu hospitalier a permis de côtoyer dès 1980 de nombreux chirurgiens utilisateurs de lasers médicaux adaptés à leurs spécialités. La particularité de certains rayonnements pouvant pénétrer en profondeur dans les tissus cibles, a semblé intéressante pour atteindre les tissus parodontaux infectés en profondeur. Dans les parodontites agressives, nous connaissions une résistance des antibiotiques et le pouvoir de pénétration des bactéries pathogènes ne permettait pas d’assainir les poches infectées à l’aide d’un simple curetage chirurgical.
Il est donc décidé d’étudier les rayonnements lasers et leurs éventuelles possibilités médicales (Fig. 6).
C’est au cours de déplacements lointains qu’un premier rapprochement est effectué avec des industriels spécialisés dans les technologies lasers.

Fig. 6 - L’intérêt des lasers me semblait au départ de pouvoir atteindre les zones profondes à l’aide d’un rayonnement pénétrant
Les nombreuses lectures disponibles sur le sujet, laissaient supposer à l’époque que nous pouvions trouver des possibilités de décontamination grâce aux rayonnements lasers :
L’Université de Seattle en 1997 …. L’Université de Vienne en 1998 …. L’Université de Tokyo en 1996 …. Tous indiquent que les rayonnements des lasers Nd YAG, Diodes, et même Er YAG ont des pouvoirs bactéricides sur les pathogènes bucco-dentaires (Fig. 7) (Moritz et al. 1997) (Tseng P et al. 1991) (Ando Y et al. 1996).
Les premiers tests cliniques sont donc effectués avec comme seules références cette bibliographie, et le mode d’emploi de la machine ….
Les résultats sont particulièrement décevants, les contrôles effectués en postopératoire ne montrent aucune amélioration dans la quantité ou la qualité des pathogènes présents initialement (Fig. 7.2).
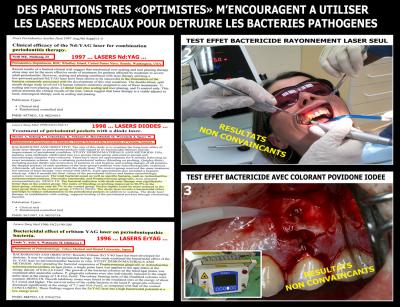
Fig. 7 – Les parutions des années 96, 97 et 98 faisaient preuve d’un optimisme peu réaliste
Seul un effet thermique relativement fort, qui a un effet destructeur aussi bien sur les tissus vivants que sur les tissus infectés, permet d’obtenir une disparition des bactéries par stress thermique, ce qui n’est pas du tout le but recherché !
Il est nécessaire de tester d’autres pistes particulièrement avec la photothérapie dynamique et l’utilisation de colorants. (Gursoy H et col. 2013)
Dans ces essais non plus, les résultats ne sont pas convaincants. Le colorant bloque le rayonnement laser et l’empêche de pénétrer dans la profondeur des tissus où se trouvent des concentrations bactériennes, parfaitement protégées de l’action photodynamique (Fig. 7.3).

Fig. 8 - Evolution de la technologie lasers entre 1997 et 2010
A l’époque, beaucoup des lasers testés sont extrêmement thermiques et difficilement réglables. Leur utilisation nécessite expérience, prudence et gestuelle adaptée.
D. ETUDES DES PROPRIÉTÉS DES LASERS MÉDICAUX
Pour tenter d’améliorer, il faut comprendre la machine. Ceci est effectué par de nombreuses lectures et formations en transformant le cabinet médical en laboratoire de tests lorsque l’emploi du temps le permet (Fig. 8).
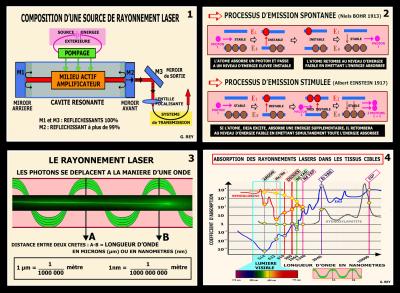
Fig. 9 - Les principes physiques de base permettent de comprendre le rayonnement lasers
Le principe d’émission stimulée décrit par Albert Einstein étant acquis (Fig. 9.2), on comprend vite l’amplification dans la cavité résonnante et la prise en charge par le système de transmission jusqu’aux tissus cibles (Fig. 9.1).
A la sortie, le rayonnement souvent invisible, se déplace comme une onde dont la longueur d’onde définit sa position sur le spectre électromagnétique (Fig. 9.4). (Chavoin JP et al. 1995)
C’est cette particularité qui permettra de différencier les lasers en rayonnements absorbés non pénétrants (CO2, Er:YAG, Er:Cr,YSGG) et en rayonnements pénétrants absorbés dans la profondeur des tissus cibles (Nd:YAG, Nd:Yap, Diodes) (Fig. 11).
Nous obtenons donc soit une action superficielle, soit une action en profondeur en fonction de la longueur d’onde du rayonnement laser utilisé (Fig. 10.1-2-4).
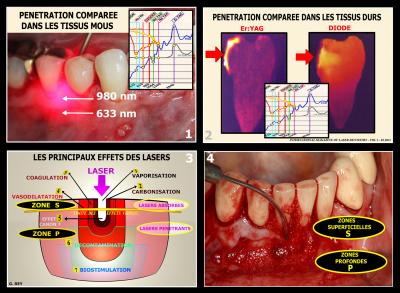
Fig. 10 - La pénétration différente des rayonnements permet de les classer en lasers non pénétrants et en lasers pénétrants.
Les effets des lasers peuvent être soit des effets thermiques plus ou moins forts, soit des effets de vaporisation (thermiques très forts) et dans la profondeur des tissus, l’absorption de l’énergie photonique permet une biostimulation cellulaire et sous certaines conditions, une décontamination des zones infectées ((Fig. 10.3). (Rey G, Missika P. 2010)

Fig. 11 - Représentation des deux familles de lasers : lasers absorbés et lasers pénétrants
E. DECOUVERTE DE LA PHOTO-THERAPIE DYNAMIQUE SANS COLORANT
Une bonne connaissance de la bactériologie bucco-dentaire est nécessaire dans un exercice médico-dentaire moderne. L’utilisation d’un microscope à contraste de phase permet une analyse de la flore sous gingivale visible (Fig. 12).
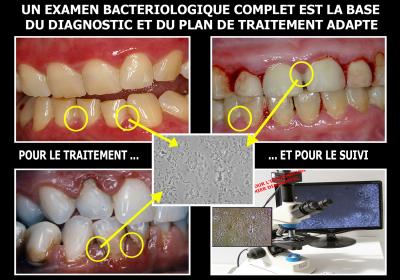
Fig. 12 - Le microscope bactériologique est un outil de prévention et de maintenance indispensable
La lecture de nombreux ouvrages sur la bactériologie clinique et les connaissances acquises en Chine ont permis de mieux comprendre l’influence des bactéries pathogènes bucco-dentaires sur la santé générale (Fig. 13.1).
De nombreuse bactéries diffusent au travers de l’organisme et peuvent provoquer des endocardites, des infections généralisées, des infections pulmonaires, des infections abdominales ou uro-génitales, des infections du cerveau, du sinus, des oreilles, etc. ….
C’est toute l’importance du rôle de prévention de la médecine dentaire moderne qui permet, grâce à une bonne collaboration avec les confrères médecins, d’aider à la guérison de pathologies très éloignées de la cavité bucco-dentaire. (Avril JL et al. 2000)
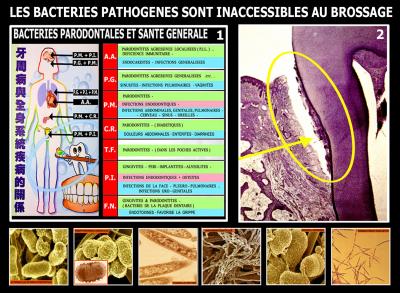
Fig. 13 - Influence des bactéries pathogènes bucco-dentaires sur la santé générale
Les bactéries microscopiques sont présentes sous la gencive et dans les poches parodontales profondes (Fig. 13.2). (Socransky et al. 2000)
Lorsqu’elles sont dans des lésions osseuses, elles sont inaccessibles au brossage et la prévention nécessitera l’utilisation d’un instrument complémentaire : hydropulseur. Celui-ci sera indispensable pour assainir l’ensemble des zones sous gingivales.
Au-delà des lésions parodontales décelables par sondage ou radiographie, les tissus gingivaux et osseux voisins sont également envahis par les bactéries pathogènes.
Un curetage, aussi méticuleux soit-il, ne permet pas d’assainir ces tissus parodontaux en profondeur.
Les lésions sont les conséquences de l’infection parodontale, les causes sont des proliférations bactériennes dans l’ensemble du parodonte. Ce sont ces causes qu’il convient de traiter en priorité (Fig. 14).
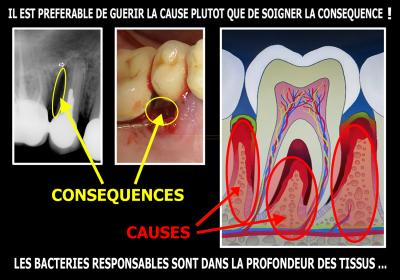
Fig. 14 - Pour guérir une pathologie, il vaut mieux s’adresser aux causes qu’aux conséquences
Nous comprenons qu’un laser pénétrant est nécessaire pour atteindre les causes des maladies infectieuses parodontales, dans la limite de pénétration du rayonnement qui peut atteindre ou dépasser 15 ou 20 mm dans certaines conditions.
Les bactéries pathogènes étant principalement anaérobies ou mixtes, il est décidé d’oxygéner préalablement les tissus avant d’appliquer une irradiation avec un rayonnement laser pénétrant. La présence de peroxyde d’hydrogène à 3 % dans les lésions parodontales irradiées permet de réduire également l’effet thermique de ce rayonnement sur les tissus cibles.
Pendant la première année de tests, ce traitement laser sous eau oxygénée est mis en place uniquement après un échec du traitement classique effectué par curetage et antibiothérapie (Fig.15).
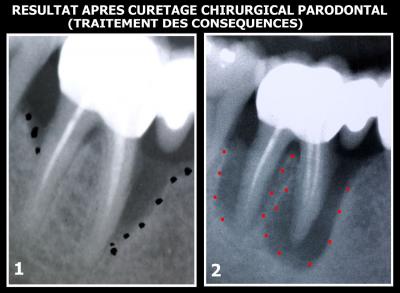
Fig. 15 - Echec d’un traitement classique par curetage
C’est le cas pour cette molaire 46 :
De l’eau oxygénée à 10 vol. est déposée dans la profondeur des lésions de cette molaire. Nous laissons les tissus s’oxygéner et nous irradions ensuite avec un laser Diode réglé en mode Pulsé et une puissance qui permet de maitriser les effets thermiques au niveau de la vasodilatation.
Cette énergie photonique propulsée sur des tissus préalablement oxygénés, crée conjointement plusieurs types de réactions :
-
Des réactions photochimiques (activation d’une substance par un rayonnement)
-
Une photothérapie dynamique (transformation de la matière sous l’effet d’une énergie lumineuse) sur les tissus cibles oxygénés mais colorés au départ par la présence d’hémoglobine ou de mélanine (Fig. 16).
Ces réactions de photo-oxydation en présence d’oxygène permettent la création d’oxygène singulet et d’oxygène triplet qui semble être à l’origine des résultats constatés. (Rey G, Missika P. 2011)
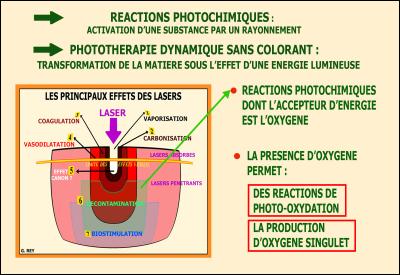
Fig. 16 - La présence d’oxygène est nécessaire pour obtenir les réactions photochimiques et l’effet décontaminant
Le traitement se fait sans chirurgie, uniquement par dépôt de peroxyde d’hydrogène à 3 %, puis par irradiation avec un rayonnement laser pénétrant (ici laser Diode).
Le résultat est une disparition de l’infection visible cliniquement très rapidement, suivi d’une guérison progressive des tissus parodontaux. Cette guérison des tissus osseux est évidemment assujettie à une bonne prévention (hygiène bucco-dentaire et surveillance par maintenance). (Rey G. 2000)
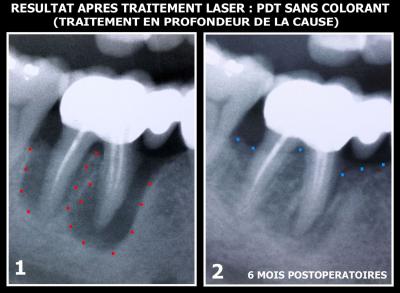
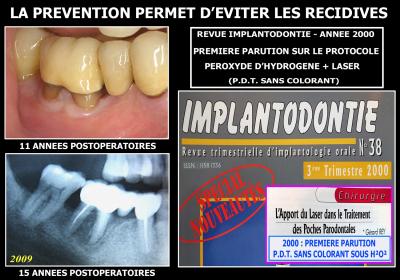
Fig. 17 - A 6 mois postopératoires, la reconstruction osseuse est correcte
Plusieurs cas identiques effectués dans les mêmes conditions dans les années 90, ont permis une première parution sur les résultats obtenus par le rayonnement laser utilisé sans colorant dans la revue « Implantodontie » N°38 du 3ème trimestre 2000 (Fig. 18).
Cette technique est dénommée : « La Photothérapie sans colorant » pour la différencier de la P.D.T. classique qui prévoit l’injection ou le dépôt de substances photo-sensibilisantes avant l’irradiation lumineuse.
Fig. 18 - Première parution sur le protocole Photothérapie sans colorant : 3ème trimestre 2000
Le patient est revu à 11 années postopératoires, puis à 15 années postopératoires, avec un état clinique tout à fait stabilisé.
Il continue une hygiène bucco-dentaire de prévention stricte et nécessaire. Les maladies parodontales agressives sont des maladies infectieuses qui peuvent toujours récidiver comme n’importe quelle maladie infectieuse, et les bactéries pathogènes résiduelles possèdent une « mémoire » (Quorum Sensing) qui facilite éventuellement cette récidive.
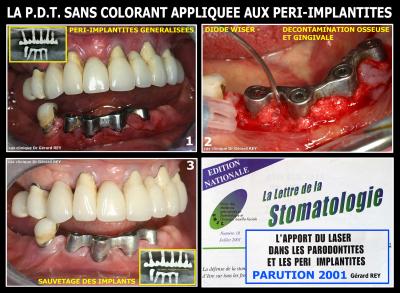
Les maladies péri-implantaires sont ensuite traitées suivant la même technique, le protocole étant légèrement différent (traitement à ciel ouvert avec un lambeau d’accès). REY G. 2001) (REY G. 2008)
Dans le cas de péri-implantites, le résultat obtenu est souvent très bon avec des reconstructions osseuses satisfaisantes. La première parution est donc complétée par une seconde dans la « Lettre de la Stomatologie » n°10 – Juillet 2001 qui détermine le protocole Lasers assisté sans colorant dans le traitement des Parodontites et des péri-implantites (Fig. 19).
Fig. 19 - Première parution sur le traitement des peri-implantites : juillet 2001
F. VERIFICATION IN VITRO EN LABORATOIRE
Dès l’année 2001, des tests in vitro certifiés par Laboratoires permettent de vérifier la réalité des constatations cliniques précédentes.
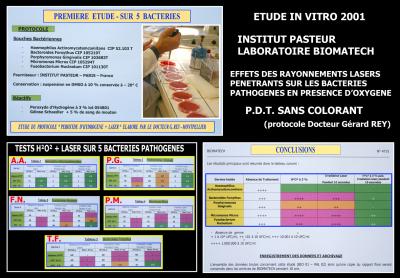
La première étude réalisée sur 5 bactéries parodonto-pathogènes majeures, en collaboration avec l’Institut Pasteur de Paris est réalisée sous le contrôle du Laboratoire Biomatech (Fig. 20).
Cette recherche démontre qu’une seule bactérie est sensible en réalité aux rayonnements laser et au Peroxyde d’hydrogène : Aggregatibacter actinomycetemcomitans.
Toutes les autres, Tannerella forsythia, Porphiromonas gingivalis, Peptostreptococus micros et Fusobacterium nucleatum ne sont sensibles ni au Peroxyde d’Hydrogène à 3 %, ni aux rayonnements laser. (Etudes Laboratoires Biomatech – Fournisseur Pasteur 2001 – sur protocole Dr Gérard REY)
Par contre, l’effet bactéricide est réel lorsque l’on additionne la présence d’eau oxygénée à 10 volumes et l’irradiation par un rayonnement laser.
Fig. 20 - Première étude in vitro en 2001 sous contrôle des Laboratoires
D’autres études suivront dont certaines en collaboration avec le Pr Gianluigi Caccianiga, l’Université de Milan Bicocca et le service du Professeur Tredici. Et une autre également en France, avec l’Institut Alfred Fournier sur le même protocole utilisé avec de nouveaux lasers diodes. (810 et 980 nm).
Sur cette étude de l’Institut Alfred Fournier, il est démontré qu’aucune bactérie pathogène n’est sensible aux rayonnements laser, que la bactérie Prevotella intermedia est sensible au Peroxyde d’hydrogène à 3 % et que l’ensemble des bactéries testées est également sensible au protocole « Peroxyde d’Hydrogène + Laser » avec une diminution bactérienne variant de 99,95 % à 100 % (Fig. 21). (Etudes Laboratoires Fournier 2004 sur Protocole Docteur Gérard REY).
Note : la bactérie Peptostreptococus micros s’avère plus résistante que les autres pathogènes et nécessite une puissance plus importante pour obtenir un résultat correct.

Fig. 21 - Etudes in vitro en 2004 avec l’Institut Alfred Fournier
Ces tests effectués in vitro ont permis de mieux comprendre l’effet bactéricide des lasers utilisés seuls, qui est totalement inefficace sauf sur la bactérie A.A. (nous voilà bien éloignés des parutions faites dans les années 96-97-98 par différentes universités …) (Fig. 22).
Note : Seules deux bactéries sont sensibles au Peroxyde d’hydrogène (A.A. – P.I.), une seule est sensible au rayonnement laser (A.A.) et l’ensemble des bactéries parodonto-pathogènes sont sensibles au protocole « Peroxyde d’hydrogène + laser » avec une résistance plus importante pour Peptostreptococus micros qui nécessite une durée d’irradiation et une puissance augmentées pour détruire ce pathogène.
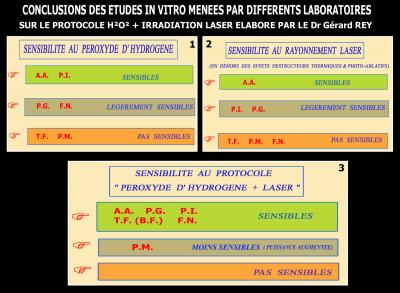
Fig. 22 - Conclusions des études in vitro sur le protocole du Dr Gérard REY
« Utilisation du rayonnement laser sans colorant »
G. LES CONSTATATIONS CLINIQUES IN VIVO
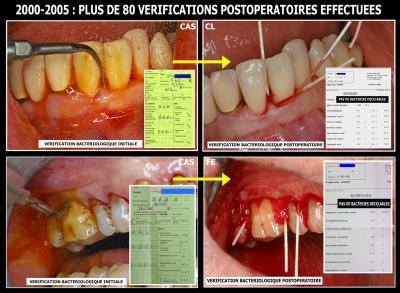
Pendant de nombreuses années, de multiples lasers ont fait l’objet d’études cliniques avec vérifications bactériologiques en postopératoires.
Fig. 23 - Tests et contrôles bactériologiques sur 5 lasers différents
Chaque patient fait l’objet d’une étude bactériologique initiale sous microscope à contraste de phase avec vérification par sonde ADN.
Après traitement, suivant le protocole défini, « H2O2 + Laser sans colorant » le même patient fait l’objet d’une vérification bactériologique par culture pour déceler les pathogènes vivants en postopératoire.
Toutes les cultures effectuées sont restées négatives après le traitement laser sous Peroxyde d’hydrogène avec l’utilisation des rayonnements pénétrants. Par contre, tous les tests effectués par les confrères du « Diplôme Universitaire Européen en Chirurgie dentaire Lasers assistée » ont confirmé que les lasers non pénétrants n’ont aucune action bactéricide efficace dans la profondeur des tissus parodontaux.
Fig. 24 - Les vérifications bactériologiques en postopératoire immédiat montrent l’efficacité réelle du protocole
avec l’utilisation d’un rayonnement pénétrant
NOTE : D’autres vérifications bactériologiques sont effectuées sur 50 patients à 6 mois, 12 mois et 24 mois.
Dans ces conditions, le résultat dépend également de la maitrise de l’hygiène bucco-dentaire après traitement. Sur ce groupe de 50 patients, 84 % ont un prélèvement négatif et 16 % avec réapparition de Fusobacterium nucleatum ou Peptostreptococus micros, sans que cela empêche la cicatrisation parodontale. Les bactéries du complexe rouge de Socransky ont, elles, totalement disparu, sous réserve de maintenir la prévention des récidives par une hygiène bucco-dentaire adaptée.
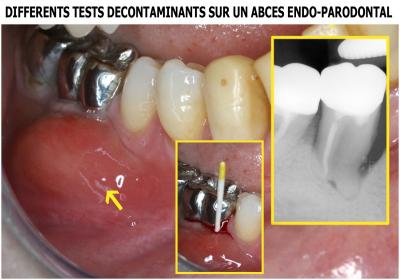
Plusieurs études sont menées avec vérification bactériologique à chaque étape du protocole pour vérifier l’instant où a lieu l’effet bactéricide décontaminant (Fig. 25 à 32) :
Fig. 25
Fig. 26
Ce patient est victime d’un abcès aigu au niveau de la molaire 46
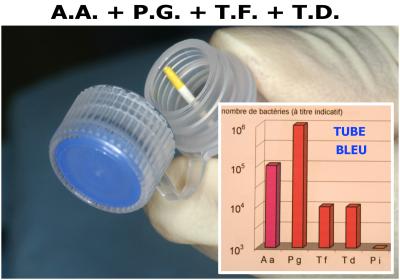
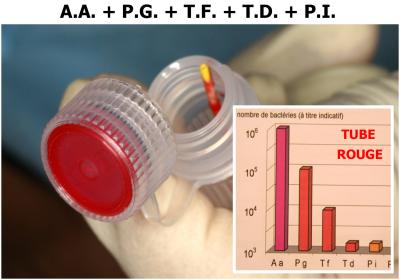
Une étude bactériologique est faite immédiatement en préopératoire (tube bleu). Le résultat montre la présence l’ensemble du complexe rouge (P.G. – T.F. – T.D.) et une quantité importante de A.A. (Fig. 26).
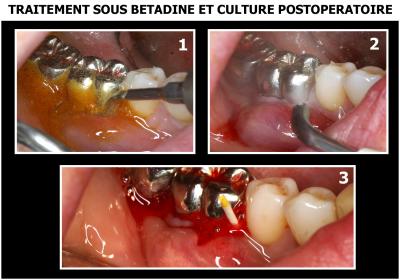
Après une anesthésie locale, ce patient subit une préparation ultrasonique sous povidone iodée, suivie de curetage et aéropolissage minutieux (Fig. 27).
Cette préparation initiale étant terminée, une vérification par culture est effectuée (tube rouge) (Fig. 28).
L’ensemble des bactéries initiales sont toujours présentes dans les lésions parodontales avec en plus une petite quantité de Prevotella intermedia qui n’avait pas été décelée initialement.
Fig. 27 - Préparation initiale sous povidone iodée
Fig. 28 - Vérification bactériologique par culture
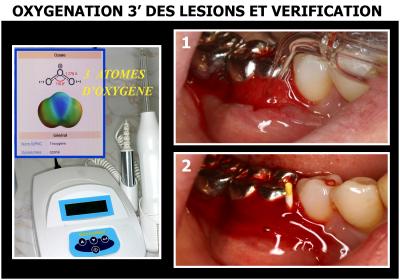
Une oxygénation de l’ensemble des lésions est ensuite effectuée pendant un temps très long de plus de 3 minutes, cette oxygénation est effectuée avec un Ozonymed (dégagement d’ozone) (Fig. 29.1).
Fig. A29 - Oxygénation avec un Ozonymed Fig. A30 - Vérification après oxygénation (Fabrication d’ozone)
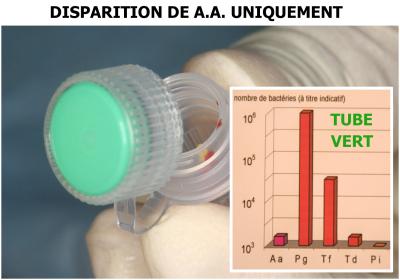
Après cette oxygénation, une culture est effectuée (tube vert) (Fig. 30).
Cette culture montre la disparition de la bactérie Aggregatibacter actinomycetemcomitans, ce qui confirme sa sensibilité au Peroxyde d’hydrogène. Par contre, les bactéries du complexe rouge sont toujours présentes.
Nous effectuons enfin uniquement une irradiation laser (Fig. 31.1) avec un laser pénétrant en mode pulsé (6000 Hz) afin de créer un maximum de cycles :
Dioxygène O2 Diamagnétique O2 Paramagnétique Dioxygène.
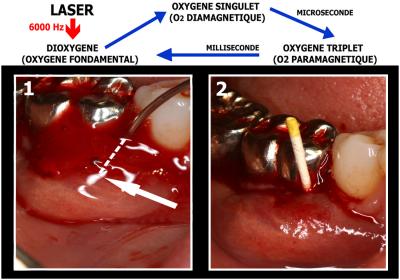
Fig. 31
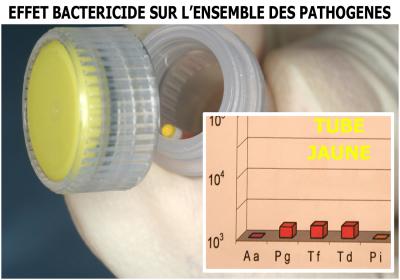
Fig. 32
Irradiation laser et vérification bactériologique (tube jaune)
La vérification par culture de ce tube jaune montre enfin une diminution quasi totale des bactéries du complexe rouge de Socransky (Fig. 32).
Il est ainsi vérifié que seul le rayonnement laser appliqué sur des tissus oxygénés détruit les pathogènes parodontaux dans ce protocole de traitement.
Par la suite, le traitement par photothérapie dynamique sans colorant sera systématiquement appliqué dans tous les traitements parodontaux avec des résultats tout à fait encourageants (Fig. 33).
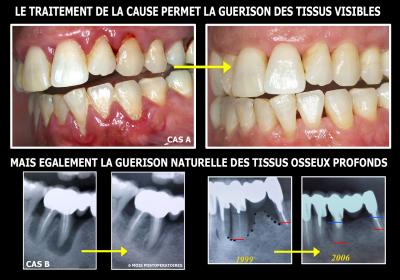
Fig. 33 - Le simple traitement des bactéries responsables permet la cicatrisation des tissus gingivaux et osseux.
Ce protocole est aujourd’hui enseigné dans de nombreux pays et dernièrement les confrères italiens ont effectué une vérification des résultats obtenus par des praticiens libéraux dans leurs cabinets.
Les résultats obtenus nous montrent des diminutions variant de 76 à 99 % pour les bactéries pathogènes chez l’ensemble de ces praticiens italiens libéraux et indépendants (Pr Caccianiga – Univ. Milan Bicocca).