Regénérations Osseuses Guidées (ROG) : réflexions et analyse rétrospective
![]() Le patient a tendance à considérer comme normal que le traitement implantaire réussisse, magré le fréquent recours au biomatériau pour palier à l'insuffisance de volume osseux et de tissu gingival. Nous avons aujourd'hui une expérience de la pose de biomatériau et des Régénérations Osseuses Guidées (ROG). Réflexions, analyse et reflet d'expérience par le Dr Carole Leconte.
Le patient a tendance à considérer comme normal que le traitement implantaire réussisse, magré le fréquent recours au biomatériau pour palier à l'insuffisance de volume osseux et de tissu gingival. Nous avons aujourd'hui une expérience de la pose de biomatériau et des Régénérations Osseuses Guidées (ROG). Réflexions, analyse et reflet d'expérience par le Dr Carole Leconte.
Auteur : Dr Carole Leconte (Paris)
Entre hier et aujourd’hui
Loin d’avoir commencées il y a une trentaine d’années, les Régénérations Osseuses Guidées (ROG) retrouvent leurs origines dans les premières utilisations de xénogreffes en 1668 par le Pr Van Meek’ren (Neerlandais). Ce dernier réalisait des xénogreffes de voûte crânienne à partir d’un crâne de chien. En 1867: Pr Ollier (Lyon) utilisait les premières allogreffes, décrites dans son « Traité expérimental et clinique de la régénération des os et de la production artificielle du tissu osseux », pour lequel il reçu le Grand prix de Chirurgie, et devint Chevalier de la Légion d'honneur par Napoléon lui-même.
Les recherches constantes, la quête débridée de la matrice de régénération osseuse idéale ont donné vie à nombre de biomatériaux bien différents quand à leurs origines, compositions, nano, micro et macro-structures, ainsi que leurs traitements thermiques et chimiques de préparation.
Devant nous, un éventail de possibilités : os autogène broyé, allogreffe congelée, allogreffe déminéralisée, xénogreffe, hétérogreffes monophasées ou biphasées, dérivés d’algues….
Lire aussi du même auteur :
La table vestibulaire en question
Analyse de comblements sinusiens réalisés avec une allogreffe osseuse (BiobankTM)
Os : de la greffe à la regénération
Edentation maxillaire unitaire
Autres articles sur le sujet :
Les comblements osseux et alternatives aux comblements osseux
Un quotidien difficile à analyser
Il est difficile d’imaginer que l’expérience singulière d’un praticien concentre un recul clinique exhaustif. Nos objectifs de succès qualitatif, quantitatif et pérenne nous limitent dans l’utilisation à quelques matériaux pré-choisis qui ont fait leurs preuves dans les mains de nos pères.
Les conséquences à court ou long terme, dans le nuage d’incertitudes des impacts potentiels liés au changement d’un matériau ou d’une technique, expliquent aisément l’inertie naturelle dans notre spécialité.
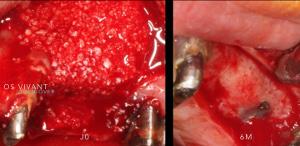
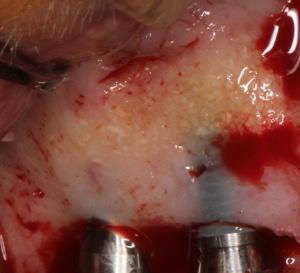
Fig 1a: Aspect clinique J0 de l’allogreffe (Biobank) mélangée au sang avant la mise en place de la membrane de collagène à résorption lente (Creos© - Nobel Biocare) stabilisées par des clous Titanes.
Fig 1b: Aspect de la néo-corticale, dure, représentant un plan de clivage avec la muqueuse. De nombreuses insertions de vaisseaux périostés sont visibles.
Le nombre sans fin de facteurs liés à la technique, à la biologie du patient, et au comportement des biomatériaux rend bien difficile les analyses et font perdre du sens à bien des méta-analyses.
De plus, analyser, dans nos expériences cliniques, l’impact spécifique du biomatériau par exemple, demande un grand nombre d’utilisations afin de percevoir des grandes lignes de comportement matériau-dépendant. Avec la prise de risque que constitue le délai entre l’utilisation, la cicatrisation, et l’évolution au fil des années.
Chaque impact, individuellement, est donc difficilement dissociable du global, mais l’expérience fini par donner de la clarté vis à vis des liens entre nos actes, nos choix et leurs conséquences.
Fig 2: Aspect d’une réouverture à 2 ans d’un sinus lift réalisé avec une xénogreffe (Biooss) mélangée au serum physiologique.
Un idéal comme guide et son alternative boostée:
Nous partirons du principe que l’os autogène broyé est idéal.
Il est souvent expliqué que ces qualités viennent de son caractère « vivant » à l’échèle cellulaire.
Dr Fouad Khoury a montré dans son expertise la nécessité de broyer la corticale et de la stabiliser dans une box biologique. Ceci ne fait plus débat tant le comportement d’un bloc cortical augmente considérablement les taux de complications et échecs.
Cependant, Dr Guillaume (2009) a montré que dans le cadre d’un prélèvement autogène que 80% des ostéocytes étaient déjà morts 20 mn après le prélèvement. En même temps, peu importe, les ostéoblastes ne proviennent pas des ostéocytes du greffon prélevé, mais des progéniteurs du patient (cellules souches différenciées).
Alors quel bénéfice vis à vis de biomatériaux?
L’os du patient bénéficie des médiateurs chimiques libérés par l’apoptose des cellules, mais principalement du collagène et des protéines constitutionnelles du greffon.
Ainsi, des biomatériaux comme les allogreffes, respectant la structure minérale et collagénique présentent un avantage certain de similitude.
Le mode de traitement chimique et thermique a cependant un rôle capital dans la préservation des propriétés biologiques et physiques du biomatériau d'origine osseuse.
Dr Vastel en 2004, 2009 a montré la supériorité du procédé Supercrit® pour la préservation de la résistance biomécanique.
Un élément de traitement bien souvent éludé est très important quand on parle de biomatériaux : le taux de lipides résiduels. En effet, les procédés de préparation des allogreffes vont être plus ou moins efficaces pour éliminer les lipides de la moelle osseuse. Il est connu que les lipides résiduels des allogreffes sont un véritable poison cellulaire (Dr Moreau, 2000).
Ceci vient de la péroxydation des lipides lors de la stérilisation par rayonnements gamma (norme de stérilisation) qui induit la formation de composés cytotoxiques.
Les protéines osseuses ont un rôle clef

Fig. 3a, b, c, d: Etapes du prélèvements de chips d’autogène au Safescaper qui seront mélangés à l’Allogreffe (Biobank cortico-spongieuse petites particules) puis au sang prélevé in situ.
Le manque de protéines osseuses (BMP) semble être la seule faiblesse biologique des allogreffes qualitatives versus l’autogreffe.
Cependant, un trauma chirurgical doux comme le fraisage de surface ou les perforations corticales vont provoquer la production de protéines de cicatrisation osseuse. L’emploi, si nécessaire, d’un safescraper favorisera grandement une légère hémorragie osseuse de surface, ouvrira les ostéons, et permettra la récupération d’un broya d’autogène. Ce dernier, certes peu quantitatif, est ostéo-inducteur. Il peut aisément être mélangé aux particules de biomatériau. L’allogreffe, matrice ostéoconductrice de minéral préservé, riche en collagène favorisant le clou plaquettaire et l’angiogénèse, devient ainsi biologiquement ostéo-inductrice.
L’utilisation dans le respect des règles d’une allogreffe à la structure minéralo-collagénique préservée par le procédé Supercrit©, avec stimulation osseuse semble donc pouvoir associer les intérêts irréfutables de l'os autogène broyé sans avoir les contraintes de quantité / morbidité / risque septique ou d’échauffement du site donneur. En plus, de qualité très régulière, les petites particules cortico-spongieuses associent une forte hydrophilie, véritable pompe à sang, à un comportement de matériau biphasé (résorption plus lente, meilleure densité minérale, …)
Des critères cliniques et radiologiques de succès
L’évaluation d’une ROG peut paraître ambiguë. En effet, l’utilisation d’une matrice minérale induit dès le départ un risque de confusion sur la biofonctionnalité du matériau.
Il est capital de différencier l’os natif (organe / structure vivant, avec turn-over, fabriquée par le patient), de la matrice minérale post opératoire mis en place par le chirurgien-dentiste.
Le simple fait d’obtenir du volume ne permet pas de savoir de quelle nature est le résultat.
L’objectif de reconstruire un os alvéolaire vivant et dense pour permettre une ostéo-intégration pérenne et stable dimensionnellement impose de valider une ossification autour, entre, à travers puis à la place des particules.
L’os maxillaire, est constitué de moelle osseuse (30% environ) et de travées minéralo-collagéniques.
Il est limité par une corticale périphérique.
L’activité cellulaire est modérée hors phénomènes de cicatrisation.
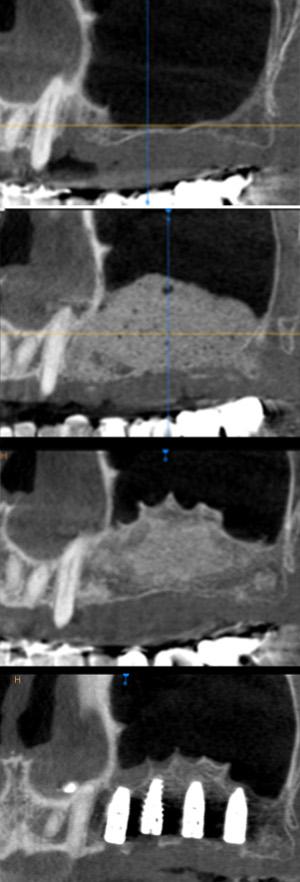
Fig 4 a à d: Madame F. Comparaison des CBCT pré-opératoires, J0, à 6 puis 9 mois. nous pouvons noter l’apparition de la néo-corticale nette, puis la trabéculation interne qui opère et évolue dans le temps. Allogreffe (Biobank) et Sang
Nous pouvons noter l’apparition de la néo-corticale nette, puis la trabéculation interne qui opère et évolue dans le temps. Allogreffe (Biobank) et Sang
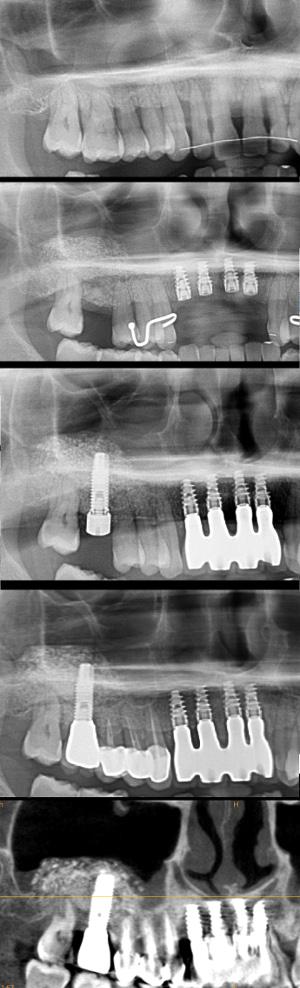
Fig 5 a à e: Comparaisons des radiographies panoramiques puis CBCT à 6 ans post-opératoire. Xénogreffe (Biooss L et serum physiologique)
Nous pouvons remarquer que 6 ans après, l’aspect est toujours hétérogène, et nous avons des signes de fibrose sur les premiers millimètres. Cependant, nous sommes en présence d’un succès du résultat implantaire.
Sur cette base, une ROG réussie conduira à une transformation visible cliniquement et radiologiquement, allant des particules à une néo-corticale.
Pour aller plus loin dans l’analyse, nous pourrons décrire les signes différenciant une fibro-intégration d’un biomatériau d’une cicatrisation osseuse réussie.
1-formation d’une néo-corticale, en continuité de la corticale adjacente du site receveur. Elle doit être formée avant les 6 mois post-opératoire.
2-disparition de l’ancienne corticale se retrouvant dans la masse de la ROG.
3-trabéculation dans la masse: son aspect interne évolue progressivement.
Lors du deuxième temps chirurgical, pour la mise en place des implants, la levée du lambeau de pleine épaisseur doit mettre en évidence un os cortical dur, rouge-crème, avec les perforations de vaisseaux périostes. Les particules ne doivent plus être différenciables.
Une analyse dynamique comparative des radiographies:
L’analyse dynamique des radiographies CBCT(« scanner » cone beam) semble être le moyen d’évaluation du succès de nos ROG, le plus simple et fiable.
Ainsi, l’absence de formation d’une néo-corticale à 6 mois, dans un cadre de persistance de particules qui restent radiologiquement individuelles, non liées par des travées, signera un échec de la ROG / sinus lift par fibrose irréversible du biomatériau.
L’histologie comme témoin
Si la clinique est parlante, elle nous joue parfois des pièges.
Aussi, il m ‘est déjà arrivé de prendre radiologiquement et cliniquement une zone de surface de ROG à 6 mois pour l’os néoformé alors que l’histologie donnait sans appel un résultat de fibrose. Certes, cette absence de cicatrisation osseuse était limitée à la surface, mais elle mettait en échec les critères conventionnels.
Dans un cadre d'une pratique quotidienne, il n’est pas envisageable de systématiser des biopsies. Cependant, bien souvent, un résultat un peu trop volumineux impliquant une résection osseuse ou alors réaliser la préparation du site implantaire avec une tréphine seront de parfaites occasions pour réaliser des analyses histologiques.
Après fixation dans le formol tamponné, décalcification, et inclusion en paraffine, le biopsie pourra avoir une coloration type HES et être analysée.
A cette échelle cellulaire, il n'y a plus de place aux doûtes. Nous allons voir la qualité du contact os néoformé / particules, la densité minérale, l’activité cellulaire…bref un instantané objectif de la vie et de la cicatrisation du site de ROG.
Selon les matériaux, les protocoles et les patients, les histologies montrent de grandes différences. Leur neutralité est un atout majeur et positionnent ces analyses comme des éléments iindispensables d’évaluation de nos reconstructions. Plusieurs laboratoires nationaux proposent ces analyses peu coûteuses, il serait dommage de s’en priver.

Fig 6: Tréphine de 2mm de diamètre interne pour biopsie/histologie
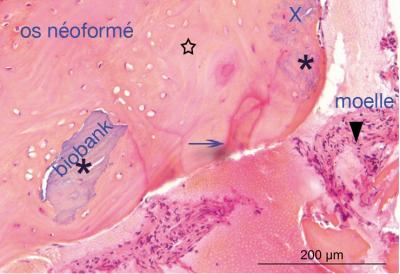
Fig 7: Madame F., Planche histologique , coloration HES.
Fig 8: Madame F, détail histologie avec legendes. Nous pouvons observer en X une particule d’allogreffe (Biobank) en cours de resorption, avec des travées d’os néoformé extrêmement intimes.
Retenons:
Si la ROG n’est qu’un acte chirurgical durant lequel nous mettons en place une matrice minérale, la cicatrisation osseuse est le phénomène biologique physiologique complexe, multifactoriel, où le corps du patient cicatrise en fabriquant de l’os. L’os néoformé alors est autour, au travers, puis progressivement à la place des particules de biomatériau.
Plus le biomatériau est bio-actif, plus la cicatrisation sera qualitative et rapide.
Notre choix se tourne vers des allogreffes à haute qualité de traitement (comme le procédé Supercrit®) mélangées au sang du patient, et mises en place sur un site receveur activé. L’utilisation du safescraper est un boost de protéines osseuses et peut compenser un saignement insuffisant.
L’analyse critique de nos réouvertures, ainsi que des radiographies CBCT à 6 mois ne doivent pas laisser de doute quant à la néoformation osseuse.
Il est capital de bien analyser les 3 critères radiologiques du succès des ROG : apparition d’une nouvelle corticale, disparition de l’ancienne corticale, et évolution de la trabéculation interne.
Plus que jamais, dans notre pratique où les volumes tissulaires
péri-implantaire ont montré leur nécessité, il faut orienter nos traitements pour stabiliser et reconstruire un os alvéolaire trophique.
Au delà d’un volume conséquent, il faut donc s’intéresser à la qualité de l’os obtenu, sa vascularisation, sa densité et stabilité.
Si les analyses cliniques et radiologiques sont le quotidien fondamental, réaliser des histologies quand cela est possible est d’un grand intérêt. Elles sont accessibles et simples à mettre en œuvre.
Il n’y a aucune technique sans succès ni échec, mais chaque technique sera plus ou moins favorable. A nous de fournir à nos patients les facteurs les plus qualitatifs tant l’impact de nos actes est grand.