Méthode d'évaluation de la cicatrisation tissulaire lors de l'implantation post-extractionnelle
 La littérature apparait discordante sur la capacité de nos traitements à optimiser le contrôle de l’architecture tissulaire dans les situations d’implantation post-extractionnelles. La problématicité de l’évaluation de la cicatrisation pourrait en être une des raisons. La pertinence de cette question est à l’origine de cet article qui propose une méthode d’évaluation à l’aide de scanners dentaires (CBCT) qui quantifie par des mesures les volumes tissulaires osseux et muqueux obtenus après cicatrisation et les compare à la situation préopératoire.
La littérature apparait discordante sur la capacité de nos traitements à optimiser le contrôle de l’architecture tissulaire dans les situations d’implantation post-extractionnelles. La problématicité de l’évaluation de la cicatrisation pourrait en être une des raisons. La pertinence de cette question est à l’origine de cet article qui propose une méthode d’évaluation à l’aide de scanners dentaires (CBCT) qui quantifie par des mesures les volumes tissulaires osseux et muqueux obtenus après cicatrisation et les compare à la situation préopératoire.
Pour consulter l'article en pdf, cliquez sur le lien en bas de page.
Parution LS 74, Juin 2017
Dr. Jean-Louis Zadikian, Dr. Jelena Stojanovic, Richard Perez, Dr. Clémence Zadikian
Extrait d’un article soumis dans une revue internationale
Lire aussi :
Variabilité du bas fon sinusien et implantation immédaite
Implantation immédiate : nouvelles possibilités thérapeutiques
Selon certains auteurs, il serait possible, dans les situations d’implantations post-extractionelles, d’optimiser le contrôle de l’architecture tissulaire 2,3,4,5,6,7,8. Le mimétisme recherché entre les tissus péri-implantaires et les tissus péri-dentaires pourrait être obtenu grâce à des techniques de régénération 2, 9, 10, 11. Cette approche viserait à compenser les pertes de volume tissulaire observées après cicatrisation au niveau d’alvéoles initialement intactes, implantées immédiatement ou pas après avoir subi les extractions. Le challenge semblerait d’autant plus élevé que la situation initiale présente une quantité importante de tissus lésés à restaurer.
La littérature apparait discordante sur la capacité de ces traitements à produire une régénération tissulaire. La problématicité de l’évaluation de la cicatrisation pourrait en être une des raisons.
La pertinence de cette question est à l’origine de cet article qui propose une méthode d’évaluation à l’aide de scanners dentaires (CBCT) qui quantifie par des mesures les volumes tissulaires osseux et muqueux obtenus après cicatrisation et les compare à la situation préopératoire. Pour soumettre les volumes des tissus mous à cette confrontation, ces scanners seront réalisés en utilisant un écarteur photographique pour tenir les lèvres et les joues à distance des dents1. Cet article n’a pas pour but de détailler l’intégralité des protocoles chirurgicaux et du matériel de régénération tissulaire utilisés.
Le cas de Frédéric, 37 ans, servira à illustrer le protocole de mesure.
Lors d’une unique session, il a subi un traitement dans lequel ont été réalisés :
Les extractions
Les implantations
Les compensations chirurgicales nécessaires à restaurer les tissus endommagés (dans le but d’atténuer les compensations prothétiques)
Une mise en charge immédiate bi-maxillaire (trois heures après la pose des implants) évitant au patient d’endurer une temporisation conventionnelle amovible 12, 13.
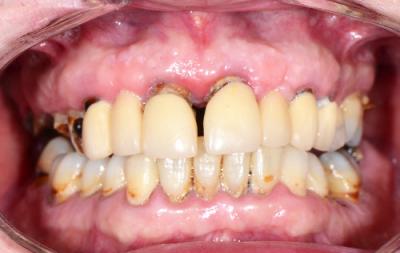
Figure 1 - Situation initiale préopératoire.
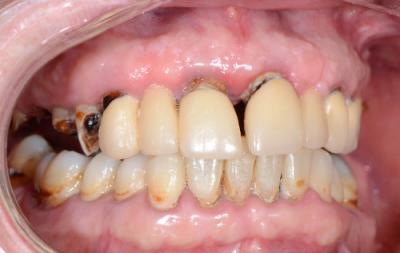
Figure 2 - Situation initiale préopératoire.
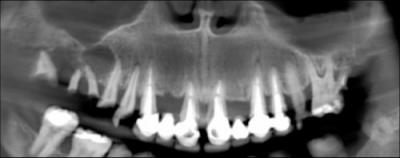
Figure 3 - Situation initiale, coupe panoramique sur le scanner dentaire préopératoire.
Frédéric présentait une parodontite chronique généralisée sévère (Fig. 1, 2 et 3) avec des désordres dentaires (mobilités, égressions, migrations), des destructions tissulaires et des troubles liés à la mastication et à l’esthétique.
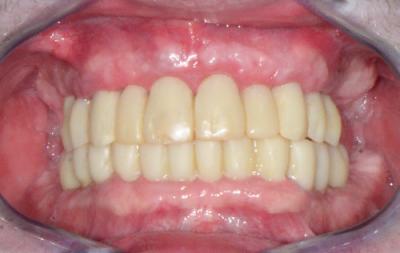
Figure 4 - Bridge provisoire à 8 mois post-opératoire.
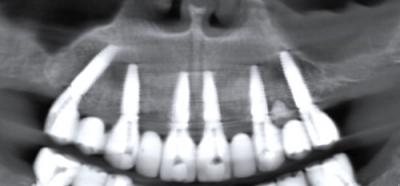
Figure 5 - Coupe panoramique sur le scanner à 8 mois post-opératoire
Les figures 4 et 5 présentent le bridge implanto-porté provisoire obtenu à 8 mois sans que le recours à une gencive prothétique ne se soit imposé (PF3). Il correspond à un PF1 de la classification de Misch14. La ligne de transition naturelle observable entre le bridge et la gencive semblerait montrer une architecture tissulaire restaurée. Toutefois cette approche descriptive ne suffit pas pour juger de la capacité de ce traitement à produire une régénération tissulaire.
1) Matériel utilisé
a) Le cas clinique de Frédéric, 37 ans, servira à illustrer le protocole de mesure, à partir d’une situation initiale préopératoire et celle à 8 mois post-opératoire (Fig. 1, 2, 3 et 3, 4 et 5).
b) Les scanners utilisés sont issus d’un scanner dentaire Cone-Beam Planmeca Promax (Planmeca Oy, Helsinki, Finlande) installé dans le cabinet du Dr. Jean-Louis ZADIKIAN. Ce scanner dispose d’un champ de 8 cm x 8 cm x 8 cm, d’une résolution de 250 x 250 x 250 voxels et d’une taille de voxel de 320 µm.
2) Méthodologie de mesure
L’analyse des images et les mesures ont été réalisées sur le logiciel de visualisation et de planification implantaire Romexis version 4.4.0 de la société Planmeca (Planmeca Oy, Helsinki, Finlande).
Comment obtenir les figure 3 et 5 qui représentent les panoramiques préopératoires et post-opératoire à partir desquelles on obtient les coupes vestibulo-palatines sur lesquelles on effectue les mesures ?
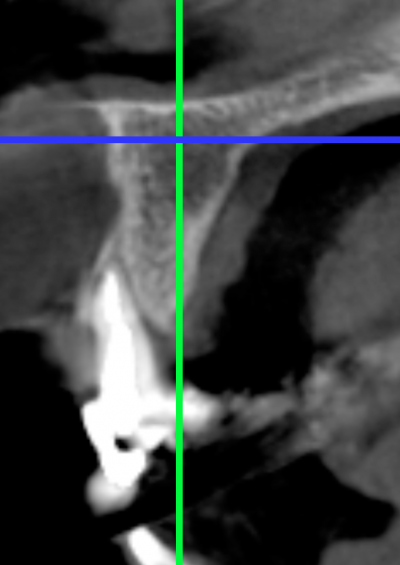
Figure 8 - Coupe V-P au niveau de 11 résultant du tracé réalisé sur la figure 7. (scanner préopératoire).
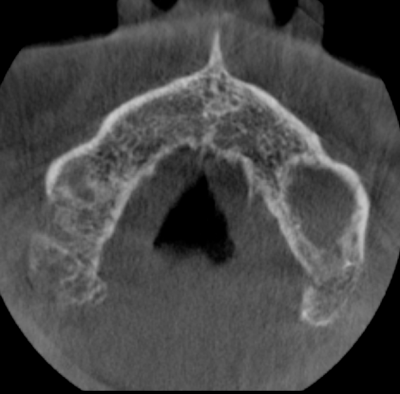
Figure 6 - Coupe axiale située à une distance de 3,20 mm du plancher des fosses nasales. (scanner préopératoire).
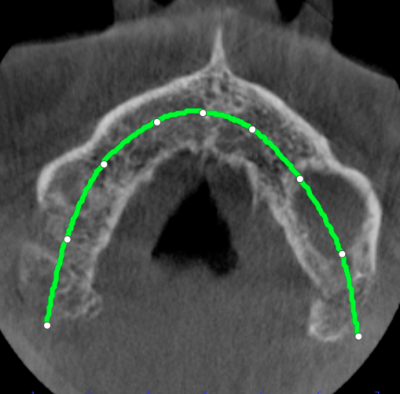
Figure 7 – Trait vert : Plan de coupe de la coupe axiale. (scanner préopératoire)
Paramétrages nécessaires à l’obtention de la figure 3 (de la Fig. 6 à la Fig. 11) :
La coupe axiale de la figure 6 a été choisie et se trouve à une distance de 3,20 mm du plancher des fosses nasales (voir niveau du trait bleu sur la figure 8). Elle doit cependant se situer en dessous du niveau de la voûte du palais sans toutefois être arrêtée dans une zone trop coronaire pour rester dans une région indemne de lésions tissulaires.
Sur cette coupe axiale, réaliser le tracé (trait vert sur la figure 7) qui permettra d’aboutir à la coupe V-P correspondante (Fig. 8). Ce tracé parcourt un chemin plutôt parallèle à la table interne et se trouve à mi-distance entre la table interne et externe pour générer la coupe V-P de la figure 8.
Cette dernière va subir une translation vestibulaire jusqu’à se superposer au plus grand axe vertical de la dent (trait vert de la figure 9), pour produire une nouvelle coupe axiale (Fig. 10).
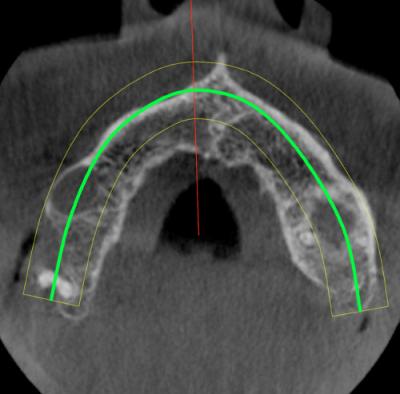
À partir de cette nouvelle coupe axiale (Fig. 10) sera effectuée une rotation de l’image.
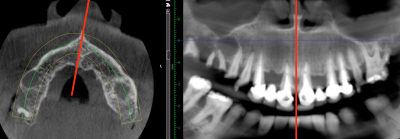
Cette rotation de l’image se fera dans le sens inverse des aiguilles d’une montre jusqu’à faire coïncider la suture intermaxillaire sur le trait rouge (Fig. 11a et b), le trait rouge (Fig. 11 b) illustrant la suture intermaxillaire correspondant aussi à la droite D1 de la figure 13.
Paramétrages nécessaires à l’obtention de la fig. 5 :
L’objectif est de pouvoir comparer les mesures relevées après la cicatrisation et celles réalisées avant l’intervention.
Le scanner à 8 mois de cicatrisation sera paramétré à partir des données acquises sur le scanner préopératoire avec un raisonnement identique pour arriver à la coupe panoramique de référence (Fig. 5 et Fig. 15)
3) Présentation du protocole de mesures :
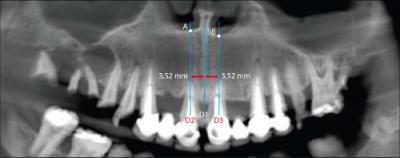
Figure 13 - Position des droites D1 et D2 sur la coupe panoramique du scanner préopératoire.
Sur la coupe panoramique du scanner préopératoire (Fig. 3), la droite D1 passe par la suture intermaxillaire (Fig. 13).
D2, droite parallèle à D1 (Fig. 13) s’inscrit sur le plus grand axe de la dent passant par l’apex de la 11 ou par le milieu M-D de la couronne de 11. Celle choisie pour Frédéric se trouve à une distance de 3,52 mm de la suture intermaxillaire.
L’intersection entre cette droite D2 et le plancher des fosses nasales va créer un point A remarquable. (Fig. 13)
D2 va générer la coupe V-P (Fig. 14) qui précise la position du point A, à l’intersection du plancher des fosses nasales et de la table externe, à partir duquel de nombreuses mesures pourront être effectuées.
Les tracés en bleu (Fig. 14) délimitent l’épaisseur de gencive rendu visible sur le scanner grâce à la technique des écarteurs photographiques1.
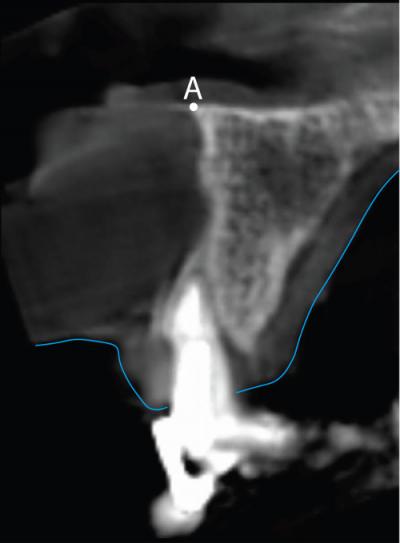
Figure 14 - Coupe V-P du scanner préopératoire correspondant à la droite D2.
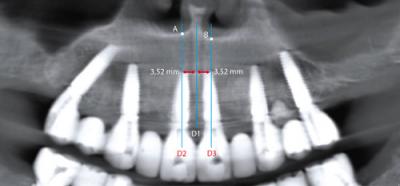
Fig. 15
À partir de la coupe panoramique (Fig. 5) sur le scanner réalisé à huit mois post-opératoire, placer à l’identique la droite D1 qui se superposera à la suture intermaxillaire (Fig. 15). D1 présente l’intérêt de se replacer de manière reproductible sur tous les différents scanners d’un même patient.
Placer à l’identique la droite D2 à 3,52 mm de D1 (Fig. 15) pour générer également une coupe VP (Fig. 16) cette fois au niveau de l’implant 11. Le point A retrouvera également sa place sur cette coupe. Cette dernière montre aussi l’épaisseur de la gencive (technique des écarteurs photographiques1).
Le point A pourrait profiter de la « notion d’invariance ». Cette hypothèse lui confère le statut de point de référence à partir duquel les mesures seront effectuées avant et après traitement et pourront être comparées.
Elles sont relevées à partir des coupes vestibulo-palatines pré-opératoires (Fig. 14) et à 8 mois de cicatrisation (Fig. 16). Les comparaisons peuvent se faire à des intervalles de temps différents en fonction des besoins de l’étude.
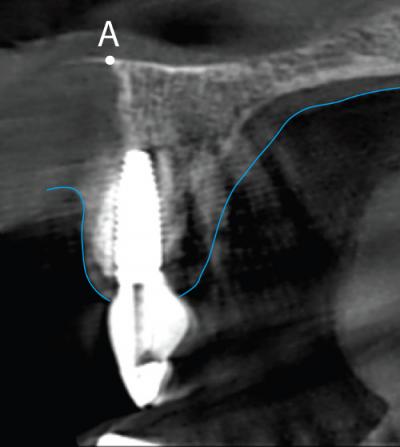
Figure 16 - Coupe V-P du scanner post-opératoire à 8 mois correspondant à la droite D2.
4) Présentation des mesures comparatives
Au niveau de 11 (Fig. 17, 18, 19 et 20)
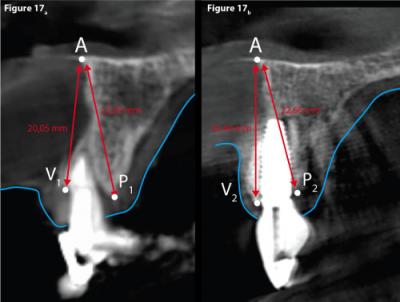
Figure 17 - Mesures comparatives des hauteurs osseuses au niveau de 11.
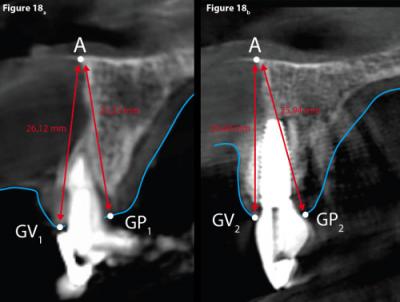
Figure 18 - Mesures comparatives des hauteurs des tissus mous au niveau de 11.
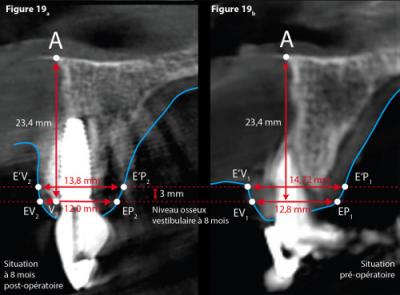
Figure 19 - Mesures comparatives des largeurs au niveau de 11.
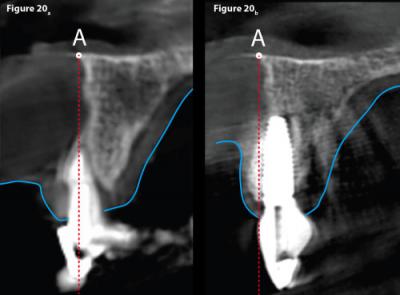
Figure 20 - Position de la dent naturelle et de la dent réhabilitée au niveau de 11.
Dans le sens vertical :
Le relevé de la distance [A-P1] = 22,60 mm et [A-P2] = 22,66 mm. (Fig. 17a et b)
Le relevé de la distance [A-V1] = 20,05 mm et [A-V2] = 23,40 mm montre un gain osseux notable d’un peu plus de 3mm. (Fig. 17)
Le relevé de la distance [A-GV1] = 26,12 mm et [A-GV2] = 25,60 mm (Fig. 18) montre une très légère perte du niveau de la gencive marginale.
Le relevé de la distance [A-GP1] = 25,23 mm et [A-GP2] = 25,94 mm (Fig. 18) montre une très légère augmentation de la gencive marginale.
Dans le sens horizontal (il est possible de réaliser des relevés à différents niveaux) :
Le relevé d’épaisseur post-opératoire : Il peut se réaliser à partir de la coupe V-P (Fig. 19a) au niveau du point V2 et à 3 mm apicalement (niveau de la table externe préopératoire)
Fig. 19a, [EV2-EP2] = 12 mm et [E’V2-E’P2] = 13,8 mm.
Le niveau du relevé d’épaisseur préopératoire : Il se réalise (Fig. 19b) en reportant à partir du point A la hauteur de 23,4 mm qui définit le point V2.
[EV1-EP1] = 12,8 mm et [E’V1-E’P1] = 14,72 mm située à 3 mm apicalement.
La figure 20a compare la position de réhabilitation de la nouvelle dent qui se trouve plus palatine (Fig. 20b) par rapport à la situation initiale.

Des relevés avec le même protocole ont été effectué au niveau de 21 (Fig.22, 23, 24 et 25)
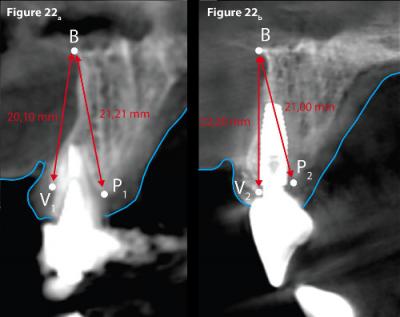
Figure 22 - Mesures comparatives des hauteurs osseuses au niveau de 21.
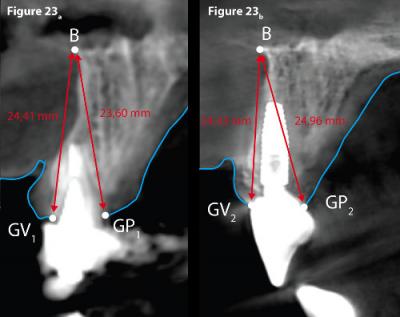
Figure 23 - Mesures comparatives des hauteurs des tissus mous au niveau de 21.
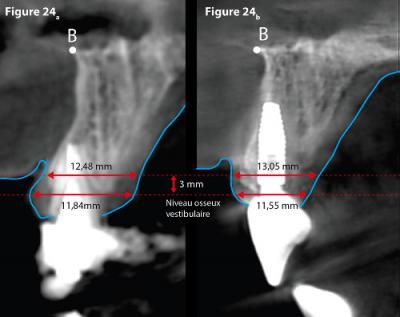
Figure 24 - Mesures comparatives des largeurs au niveau de 21.
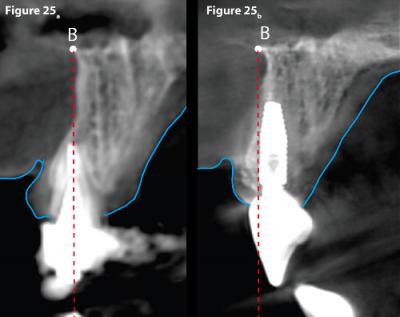
Figure 25 - Position de la dent naturelle et de la dent réhabilitée au niveau de 21.
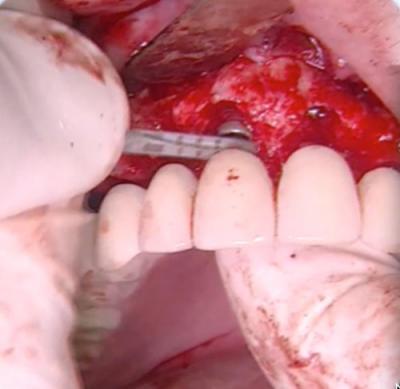
Figure 21a - Photo de la chirurgie illustrant à quelle distance l’implant a été positionné dans le sens vertical de la future dent. Relation implant-dent avec le forêt conique dont le diamètre est de 2,1 mm à son extrémité travaillante et 2,8 mm à l’autre extrémité.
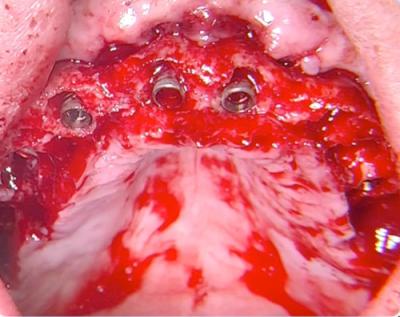
Figure 21b - Photo de la chirurgie. La relation implant-os a été obtenu grâce à la relation implant-dent pour permettre de faire évoluer la cicatrisation vers un PF1. Ce choix illustre la nécessité de réaliser une régénération tissulaire en regard des surfaces des implants non enfouies.
L’os palatin semble rester stable (distance [A-P1] = 22,60 mm et [A-P2] = 22,66 mm) (Fig. 17a et b) et Frédéric n’a pas bénéficié de régénération à ce niveau.
La table externe résorbée [A-V1] = 20,05 mm mesurée sur le scanner (Fig 17a) a bénéficiée d’une régénération.
Cette table se visualise parfaitement sur les photos (Fig. 21a et 21b) extraites de la chirurgie. Ces dernières montrent que les futures dents ont servi de guide pour que l’implant soit positionné dans le sens vertical (Fig. 21a). Pour Frédéric, la distance recherchée entre les implants, respectivement 11 et 21, avec le projet prothétique correspondant, était située entre 2,1 et 2,5 mm (cette distance correspond au diamètre du forêt conique (Fig. 21a).
En vestibulaire, une partie des spires de l’implant se trouve donc exempte d’os natif (Fig. 21b).
Après cicatrisation, à 8 mois, la valeur [A-V2] = 23,40 mm, montre un gain osseux efficace pour que les surfaces des implants non enfouies (le jour de la chirurgie) se trouvent recouverte d’os (Fig. 17b). Ce résultat établi un bénéfice osseux qui explique le résultat prothétique de PF1 obtenu. Si l’implant avait été enfoui de 3 mm la compensation prothétique aurait été réalisée avec de la gencive prothétique. La précaution eut été alors de placer la ligne de transition entre la gencive naturelle et artificielle au-dessus de la ligne de sourire. Cette situation nécessite l’enregistrement de la ligne de sourire et son transfert sur le scanner d’étude afin d’étudier comment, dans ce cas de figure, les implants seraient accueillis. Le positionnement vertical implantaire oriente le choix des options prothétiques du PF1 au PF3 mais le succès de la régénération doit être au rendez-vous pour l’alternative du PF1.
Il est a noté que, dans le sens horizontal, les mesures au niveau de V2 (Fig. 19a et Fig. 19b) nous indiquent une différence entre [EV1-EP1] = 12,8 mm et [EV2-EP2] = 12mm de 0,8 mm. Pour analyser ce résultat, il serait important de le rapprocher à ceux mesurés sur la figure 20a qui compare la position de réhabilitation des nouvelles dents (Fig. 20b) à la situation initiale. La maladie parodontale aidée de l’occlusion entraine vestibulairement les dents mais aussi les procès alvéolaires. La réhabilitation esthétique de la 11 la place plus palatine. Cette différence plaide en faveur d’une légère perte horizontale de 0,8 mm, mais cependant elle n’entraine aucune conséquence au niveau de l’harmonie entre le rose et le blanc
De la même manière, dans le sens horizontal, les mesures à 3 mm au-dessus du niveau de V2 (Fig. 19a et Fig. 19b) nous indique une différence entre [E’V2-E’P2] = 13,8 mm et [E’V1-E’P1] = 14,72 mm de 0,9 mm. Nous retrouvons de la même manière que pour [EV1-EP1] et [EV2-EP2] une légère perte horizontale n’entrainant aucune conséquence au niveau de l’harmonie entre le rose et le blanc.
Les comparaisons des mesures peuvent aussi être réalisées au milieu de la dent et en proximal sous les points de contacts dans le secteur incisivo-canin.
Conclusion
La régénération tissulaire évolue avec l’implantologie.
Dans les situations d’implantations post-extractionelles, de par sa présence, l’implant diminue le volume du défaut osseux et donc le volume à régénérer et semblerait se comporter comme un substrat ostéo-conducteur.
Son positionnement vertical oriente le choix des options prothétiques de PF1 à PF3. Il peut être considéré que le processus de cicatrisation a produit une régénération osseuse à l’aide de la technique utilisée sur ce cas clinique aboutissant à un PF1. Cette situation présente un avantage considérable au niveau de l’hygiène en la rendant plus accessible, ce qui semble être l’inverse pour une compensation prothétique PF3 importante.
Une étude17 de Lambert et al. de 2012 propose également une méthodologie de mesure des tissus osseux basé sur l’utilisation de scanners dentaires. La méthodologie expliquée dans l’article de Lambert et al. nécessite, contrairement à celle que nous proposons, d’une part la création d’un guide de positionnement permettant de placer le patient de façon identique à chaque scanner et d’autre part l’utilisation d’un logiciel spécifique permettant de « matcher » les scanners réalisés aux différents temps de l’analyse. Il résulte de la nécessité d’utilisation d’un guide de positionnement que, la méthodologie de Lambert et al. est utilisable dans des études prospective. A contrario, en nous basant sur l’étude18 de El-Beialy et al. de 2011, nous suggérons que les mesures réalisées avec la méthodologie que nous exposons sont indépendante de la position de la tête du patient et ne nécessite donc pas l’utilisation d’un guide de positionnement. Elle est donc adaptée pour une utilisation dans les études rétrospectives. Il est donc possible, sous réserve de disponibilité de scanner dentaires, de ré-analyser les résultats d’études antérieures. De plus, cette méthodologie peut se mettre en place en utilisant les fonctions usuellement disponibles dans les logiciels de planification 3D implantaires des praticiens et ne nécessite pas l’utilisation d’un logiciel supplémentaire. Il est également important de noter que notre méthodologie permet d’accéder aux mesures des tissus mous via l’utilisation d’un écarteur photographique.
La méthodologie de mesure présentée dans cet article pourrait avoir comme intérêt d’évaluer les différentes techniques de régénération. Cela aurait pour avantage de les confronter afin d’en choisir les plus prédictibles pour optimiser le contrôle de l’architecture tissulaire.
La littérature discordante sur la capacité de ces traitements à produire une régénération tissulaire ne pourrait plus se servir de l’argument de problématicité de l’évaluation de la cicatrisation.
Une étude en cours à AfopiCampus compare les résultats de 20 patients qui ont bénéficié de la même stratégie de régénération que celle utilisée dans ce cas clinique.
« Le hasard Exploite que le possible, rien que le possible, jamais l’impossible ». 15
« Le hasard diminue à mesure que la connaissance augmente ». 16
BIBLIOGRAPHIE
1) Soft tissues Cobe-Beam Compted Tomography : A novel method for the measurement of gingival tissue and the dimensions of the dentogingival unit - Januário AL, Barriviera M, Duarte WR - J Esthet Restor Dent. 2008;20(6):366- 73; discussion 374. doi: 10.1111/j.1708-8240.2008.00210.x
2) Immediate post-extraction implants with or without pure platelet-rich plasma: a 5-year follow-up study. Taschieri S, Lolato A, Ofer M, Testori T, Francetti L, Del Fabbro M. Oral Maxillofac Surg. 2017 Jun;21(2):147-157. doi: 10.1007/s10006-017-0609-2. Epub 2017 Feb 7.
3) Implant placement post extraction in esthetic single tooth sites: when immediate, when early, when late? Buser D, Chappuis V, Belser UC, Chen S. Periodontol 2000. 2017 Feb;73(1):84-102. doi: 10.1111/prd.12170.
4) Ten-year hard and soft tissue results of a pilot double-blinded randomized controlled trial on immediately loaded post-extractive implants using platform-switching concept. Canullo L, Caneva M, Tallarico M. Clin Oral Implants Res. 2016 Aug 8. doi: 10.1111/clr.12940
5) Aesthetic outcome of immediately restored single implants placed in extraction sockets and healed sites of the anterior maxilla: a retrospective study on 103 patients with 3 years of follow-up. Mangano FG, Mastrangelo P, Luongo F, Blay A, Tunchel S, Mangano C. Clin Oral Implants Res. 2017 Mar;28(3):272-282. doi: 10.1111/clr.12795. Epub 2016 Feb 23.
6) Immediate placement of single implant simultaneously with immediate loading in a fresh socket associated to periapical infection: A clinical case report. Agustín-Panadero R, Serra-Pastor B, Chust-López C, Fons-Font A, Ferreiroa A. J Clin Exp Dent. 2015 Feb 1;7(1):e175-9. doi: 10.4317/jced.52160. eCollection 2015 Feb.
7) Immediate post-extraction implants subject to immediate loading: a meta-analytic study. Enríquez-Sacristán C, Barona-Dorado C, Calvo-Guirado JL, Leco-Berrocal I, Martínez-González JM. Med Oral Patol Oral Cir Bucal. 2011 Nov 1;16(7):e919-24.
8) Outcome of single immediate implants placed in post-extraction infected and non-infected sites, restored with cemented crowns: a 3-year prospective study. Montoya-Salazar V, Castillo-Oyagüe R, Torres-Sánchez C, Lynch CD, Gutiérrez-Pérez JL, Torres-Lagares D. J Dent. 2014 Jun;42(6):645-52. doi: 10.1016/j.jdent.2014.03.008. Epub 2014 Mar 24.
9) Dental implants with versus without peri-implant bone defects treated with guided bone regeneration. Aloy-Prósper A, Peñarrocha-Oltra D, Peñarrocha-Diago M, Peñarrocha-Diago M. J Clin Exp Dent. 2015 Jul 1;7(3):e361-8. doi: 10.4317/jced.52292. eCollection 2015 Jul.
10) Clinical and immunohistochemical performance of lyophilized platelet-rich fibrin (Ly-PRF) on tissue regeneration. Zhang J, Qi X, Luo X, Li D, Wang H, Li T. Clin Implant Dent Relat Res. 2017 Feb 13. doi: 10.1111/cid.12473.
11) Cortical lamina technique: A therapeutic approach for lateral ridge augmentation using guided bone regeneration. Deepika-Penmetsa SL, Thomas R, Baron TK, Shah R, Mehta DS. J Clin Exp Dent. 2017 Jan 1;9(1):e21-e26. doi: 10.4317/jced.53008. eCollection 2017 Jan.
12) Validation of the "Quality of Life related to function, aesthetics, socialization, and thoughts about health-behavioural habits (QoLFAST-10)" scale for wearers of implant-supported fixed partial dentures. Castillo-Oyagüe R, Perea C, Suárez-García MJ, Río JD, Lynch CD, Preciado A. J Dent. 2016 Dec;55:82-91. doi: 10.1016/j.jdent.2016.10.004. Epub 2016 Oct 13.
13) Effects of new implant-retained overdentures on masticatory function, satisfaction and quality of life. Mendes FA, Borges TF, Gonçalves LC, de Oliveira TR, do Prado CJ, das Neves FD. Acta Odontol Latinoam. 2016 Sep;29(2):123-129.
14) Bone classification, training keys to implant success. Misch CE. Dent Today. 1989 May;8(4):39-44.
15) Ivar Ekeland, Professeur de mathématiques à l’Université de Paris-Dauphine
16) Anatole France.
17) A methodological approach to assessing alveolar ridge preservation procedures in humans: hard tissue profile. Lambert F, Vincent K, Vanhoutte V, Seidel L, Lecloux G, Rompen E. J Clin Periodontol. 2012 Sep;39(9):887-94. doi: 10.1111/j.1600-051X.2012.01900.x. Epub 2012 Jun 19.
18 ) Accuracy and reliability of cone-beam computed tomography measurements: Influence of head orientation. El-Beialy A, Fayed M, El-Bialy A, Mostafa Y. Am J Orthod Dentofacial Orthop. 2011 Aug;140(2):157-65. doi: 10.1016/j.ajodo.2010.03.030.