LA CHIRURGIE PRE-IMPLANTAIRE LASER ASSISTEE QUELLE LONGUEUR D’ONDE CHOISIR ?
 Quel protocole laser assisté pour une parfaite décontamination avant toute chirurgie pré-implantaire? Quelles en sont les applications en chirurgie implantaire et pré-implantaire ?
Quel protocole laser assisté pour une parfaite décontamination avant toute chirurgie pré-implantaire? Quelles en sont les applications en chirurgie implantaire et pré-implantaire ?
I. INTRODUCTION
L’implantologie n’est plus aujourd’hui un domaine réservé aux chirurgiens expérimentés et la mise en place d’implants dentaires est une réalité quotidienne pour beaucoup de praticiens correctement formés à cette nouvelle technologie dont la complexité dépend essentiellement du volume osseux initialement disponible.
La présence d’un volume osseux idéal est un facteur de réussite de l’ostéo intégration mais aussi un facteur de succès fonctionnel et esthétique dans la réalisation de la prothèse implanto portée (Bert M, Missika P. 2010)
Malheureusement nous sommes souvent en présence d’une perte du volume osseux consécutive soit à la fonte initiale de l’os de soutien, soit à la perte de l’os alvéolaire suite aux extractions dentaires, et généralement à une addition des ces deux causes.
Dans ce cas, la mise en place des implants est conditionnée à la réussite d’une chirurgie pré implantaire destinée à améliorer le volume et l’anatomie des tissus osseux résiduels initiaux.
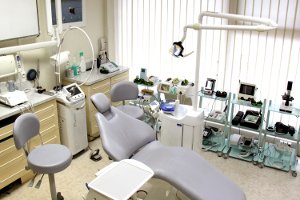
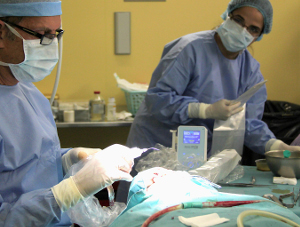
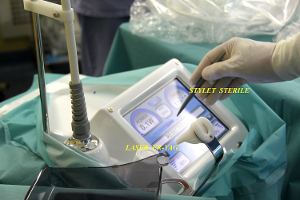
Les lasers utilisés dans nos cabinets (fig.1) ont de nombreuses applications dans le domaine de cette chirurgie pré implantaire : (Rey G, Caccianiga G 2010)
A. Décontamination initiale des maladies et infections de la cavité bucco dentaire
B. Décontamination des volumes osseux résiduels (sites receveurs) en préparation de la chirurgie reconstructrice osseuse
C. Préparation des surfaces osseuses et particulièrement pour la décorticalisation superficielle destinée à créer des échanges cellulaires entre l’os trabéculaire et les greffons mis en place.
D. Biostimulation postopératoire pour améliorer la prolifération et la différenciation des cellules mésenchymateuses (travaux de Milan Bicocca : irradiation des C.S.M. au laser pénétrant)
E. Effets ablatifs sur les tissus osseux ou sur les tissus gingivaux qui pourront être utilisés pour des actions de plastie, de découpe ou de forage et avoir un intérêt dans certains cas particuliers.
Fig.1 – Les lasers sont devenus indispensables dans nos cabinets
II. IMPORTANCE DE LA LONGUEUR D’ONDE DES DIFFERENTS LASERS
Les lasers utilisés en chirurgie dentaire se situent dans l’infrarouge avec une longueur d’onde comprise en général entre 633 nm et 10600 nm, le choix de la longueur d’onde détermine un facteur essentiel : l’absorption à la surface ou la pénétration du rayonnement dans la profondeur des tissus cibles (fig.2) (Chavoin JP, Brunetaud JM et coll 1995)
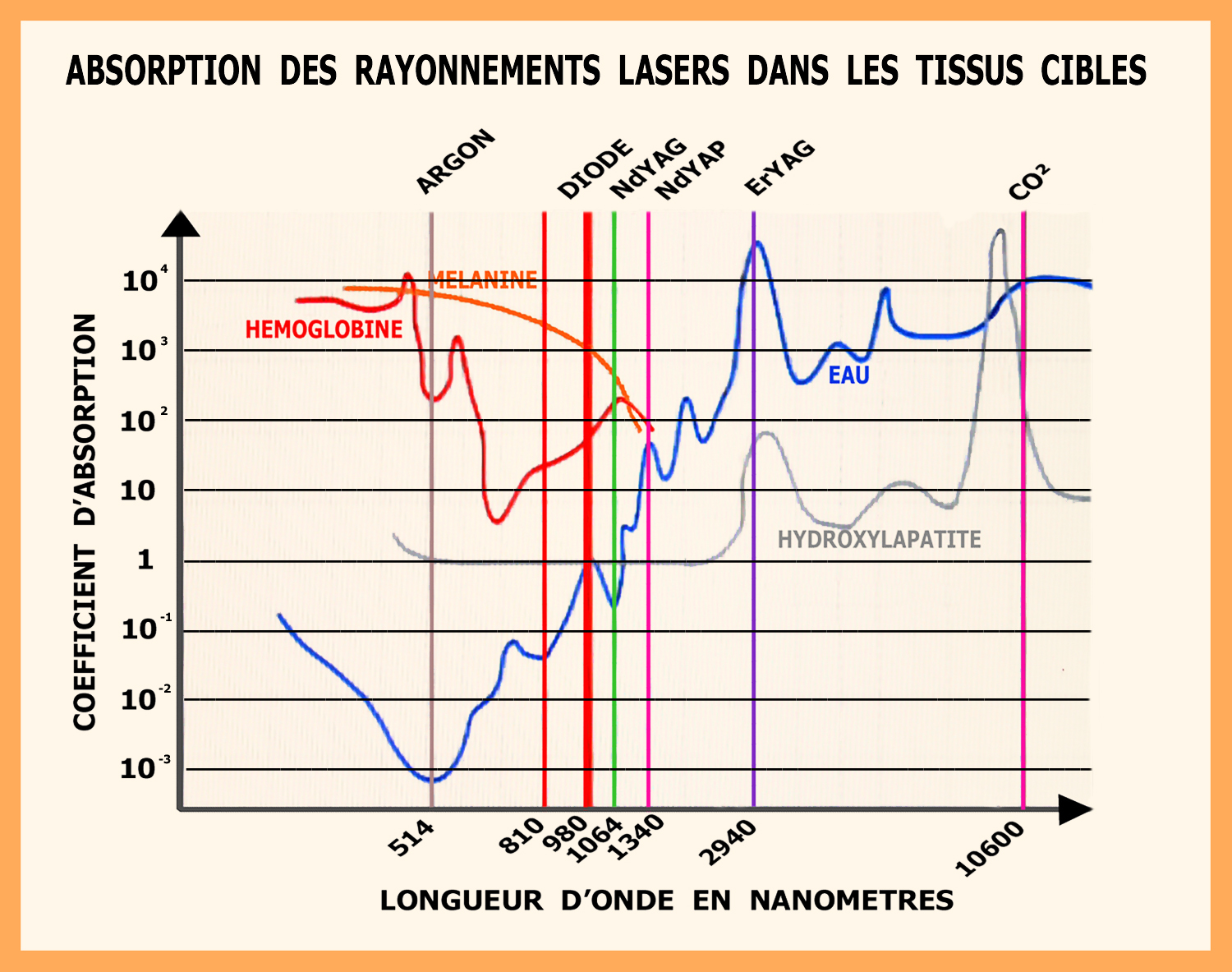
Fig.2 – Courbe d’absorption des différentes longueurs d’onde
Pour la chirurgie pré implantaire, nous avons besoin d’un laser absorbé à la surface des tissus cibles pour le traitement des surfaces osseuses résiduelles et d’un laser pénétrant pour la décontamination en profondeur et la biostimulation cellulaire des sites d’intervention. (fig.3)
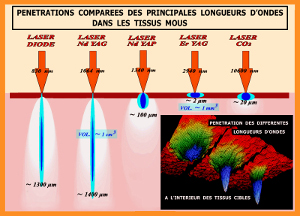
Fig.3 – Schéma comparatif de la pénétration des lasers
Le but de cette chirurgie étant l’obtention d’un nouveau volume osseux, il convient de respecter au maximum la vitalité des tissus physiologiques résiduels, nous choisissons donc les lasers qui permettent de maitriser les effets thermiques qui accompagnent systématiquement l’absorption du rayonnement laser dans les tissus cibles (fig.4)
Fig.4 – Choix des longueurs d’onde adaptées aux effets recherchés
Nous sélectionnons pour le rayonnement pénétrant un laser diode de nouvelle génération qui permet, en mode pulsé et super pulsé, un réglage précis des temps de pulse et des temps de repos, et pour le rayonnement absorbé, un laser Er YAG qui autorise une action ablative sur les tissus osseux grâce au spray de refroidissement qui accompagne le rayonnement du laser.
Nous utilisons fréquemment une diode de 980 nm (« Wiser » de Lambda – Kaelux) qui a l’avantage d’avoir une pénétration presque identique dans les tissus mous gingivaux et dans les tissus durs osseux (sa pénétration peut varier de 10 à 20 mm voire plus dans certains cas), complétée par le laser Er YAG « Pluser » d’une longueur d’onde de 2940 nm dont l’action ablative est directement visible sur la surface des tissus cibles.
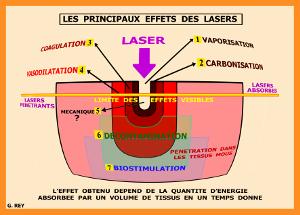
Pour la chirurgie envisagée, nous utilisons 4 effets des rayonnements lasers (fig.5) :
1/ les effets de décontamination pour la préparation initiale avant chirurgie (Rey G 2000 et 2001)
2/ les effets thermiques mais exclusivement de vasodilatation pour permettre un afflux sanguin favorable à la première cicatrisation des sites d’intervention.
3/ les effets ablatifs utilisés sous spray pour limiter l’échauffement des tissus voisins
4/ les effets biostimulants pour accélérer la cicatrisation osseuse et gingivale
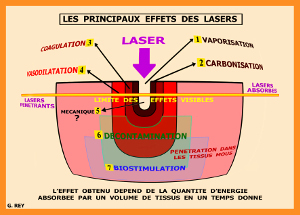
Fig.5 - Schéma des effets possibles avec les lasers médicaux
Ces différents effets doivent être utilisés en respectant la fluence nécessaire à l’action envisagée sur les tissus cibles (voir Lettre de la Stomatologie n°39)
III. OBJECTIFS DE LA CHIRURGIE PRE IMPLANTAIRE
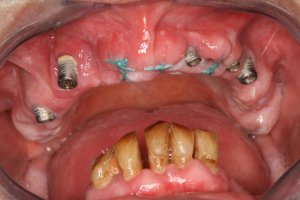
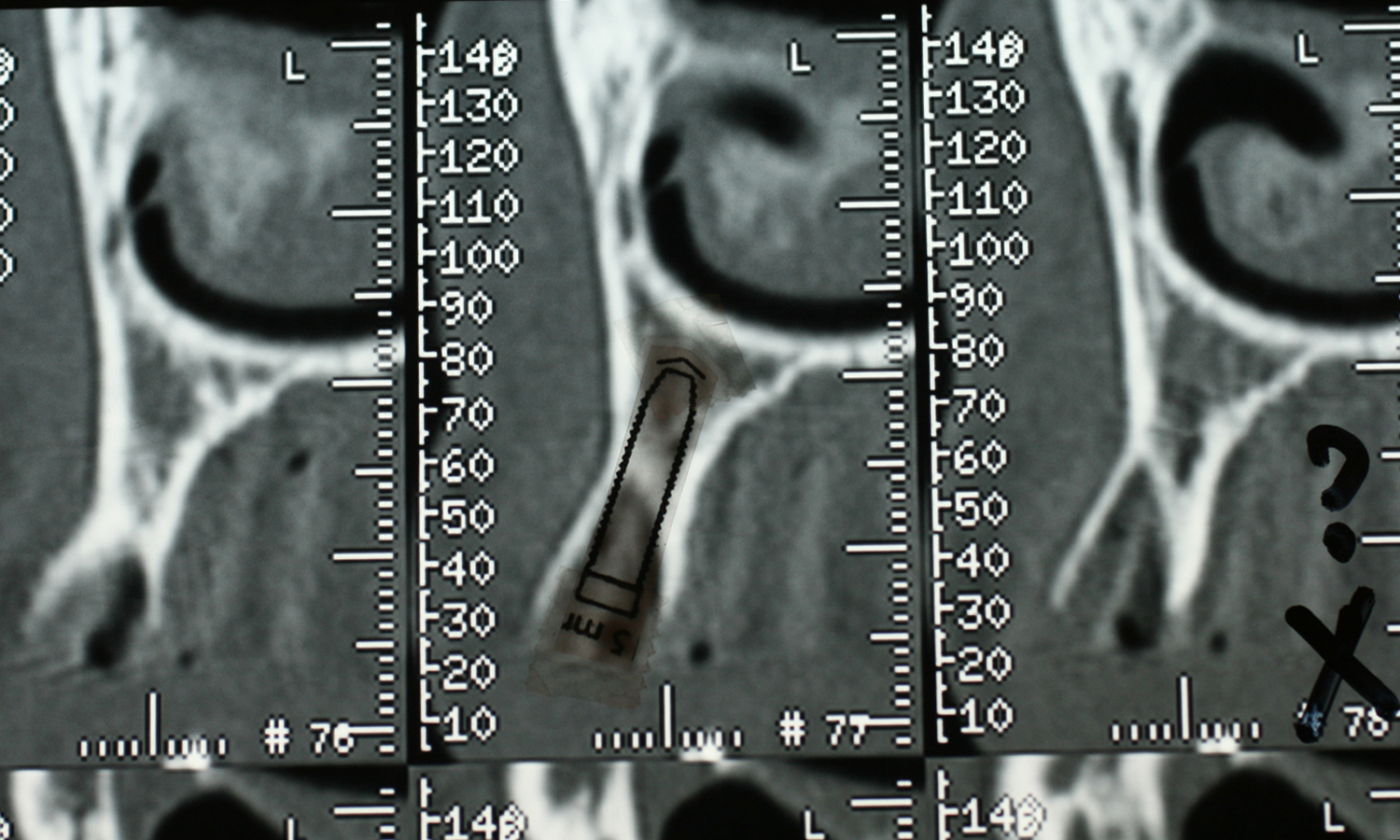
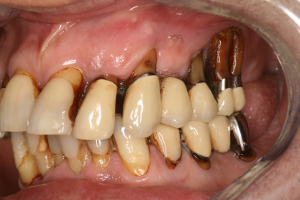
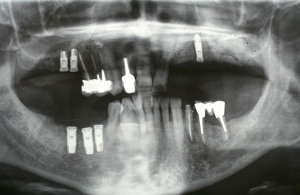
Il est possible de placer des implants sans analyse bactériologique préalable, sans étude radiographique par coupes tomographiques transaxiales, sans guide chirurgical et sans étude prothétique préalable mais le résultat risque fort de devenir celui de la figure 7 où la maladie parodontale initiale non traitée a rapidement contaminé les implants en entrainant des dégâts qui rendent impossible l’objectif de conservation des implants en raison des pertes importantes du volume osseux initial. (fig.6) (Rey G, Missika, P 2010)
Fig.6 – Le diagnostic bactériologique initial n’a pas été réalisé dans ce cas
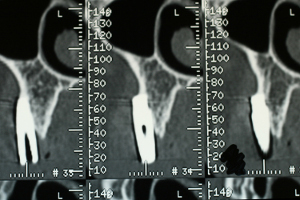
L’étude tomographique confirme le mauvais positionnement des axes implantaires (fig.7) et la finesse des volumes osseux résiduels (fig.8) qui doivent être augmentés au maxillaire et à la mandibule pour permettre la mise en place d’un nombre d’implants suffisant à la réalisation d’une prothèse fixe durable. (Khoury G, 2008)
Fig.7 - Mauvais positionnement des axes implantaires
Fig.8 – La finesse de la paroi vestibulaire impose une régénération osseuse
La chirurgie pré implantaire est réalisée dans ce cas conjointement à l’implantologie en une seule intervention.
Ceci est possible grâce à l’apport des lasers pénétrants qui permettent une décontamination immédiate de tous les tissus gingivaux et osseux de la cavité bucco dentaire.
Après extraction des anciens implants et des dents résiduelles mandibulaires, les volumes osseux maxillaire et mandibulaire sont augmentés par un apport de biomatériaux (Bio-oss + copeaux osseux autogènes + facteurs de croissance sanguins) qui permet le remodelage d’un nouveau volume osseux favorable aux tissus de soutien des 19 implants Nobel placés dans la même intervention. (Rey G, Caccianiga G et coll 2010)
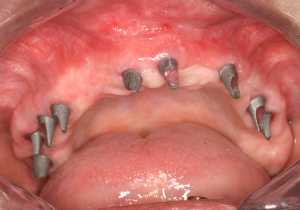
Les implants ne sont mis en fonction qu’après un délai d’attente de 8 mois (fig. 9 et 10)
Fig.9 - Mise en fonction des implants Nobel après 8 mois d’ostéointégration
Fig.10 – Equilibration provisoire pour régler la D.V.
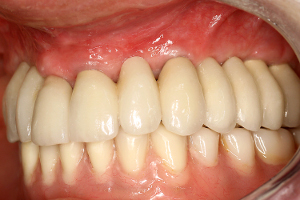
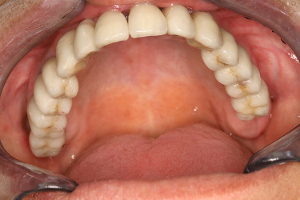
Les objectifs de la chirurgie pré implantaire ont été respectés en permettant une décontamination, une augmentation de volume et une bonne maturation des greffons avant la réalisation de 2 bridges implanto portés céramo-métalliques qui doivent faire l’objet d’une équilibration inter arcade minutieuse (fig.11 et 12)
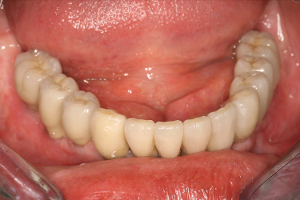
Fig.11 – Réalisation du bridge d’usage mandibulaire
Fig.12 – Réalisation du bridge d’usage maxillaire
IV. UTILISATION CLINIQUE DES EFFETS LASERS UTILES A CETTE CHIRURGIE
1. LES EFFETS OBTENUS AVEC LE LASER DIODE 980 nm
Avec ce rayonnement très pénétrant, nous devons maitriser les effets thermiques en profondeur ce qui est extrêmement facile avec le laser « Wiser » dont les paramètres ont été pré réglés suivant nos conseils et les indications liés à cette chirurgie.
Le réglage utilisé à une fréquence superpulsée pouvant aller jusqu’à 25000 Hz permet d’obtenir des photons de haute énergie accompagnés d’un effet thermique qui ne sollicite que la vasodilatation en évitant toute coagulation ou carbonisation pour conserver la vitalité des tissus irradiés.
Le premier effet concerne la décontamination obtenue sur des tissus cibles préalablement oxygénés grâce à un effet photodynamique extrêmement efficace sur toute infection dentaire ou parodontale. (Caccianiga G, Rey G et coll 2008)
Cette photothérapie dynamique (PDT) permet également la décontamination des volumes osseux avant toute chirurgie (voir Lettre de la Stomatologie n°39, n°48 et n°52)
Le deuxième effet concerne la biostimulation des tissus mous et des tissus durs qui peut être effectuée par le même laser équipé d’une lentille défocalisante provoquant un spot d’environ 1cm². Cet effet biostimulant ne doit pas entrainer un échauffement des tissus cibles supérieur à 45° ou 50°. (fig.13)
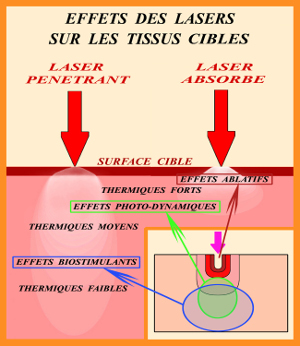
Fig.13 – Le choix du laser est fonction de l’effet recherché
2. LES EFFETS OBTENUS AVEC LE LASER ERBIUM YAG 2940 nm
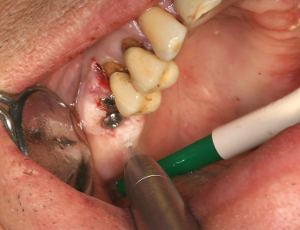
Avec ce rayonnement absorbé en surface, nous préparons les surfaces osseuses réceptrices (préalablement décontaminées) par une décorticalisation générale et la création de multiples micro cratères qui permettent de meilleurs échanges entres les tissus osseux receveurs et les biomatériaux utilisés pour lesquels nous utilisons généralement un mélange de Bio-oss (granules fins), de facteurs de croissance et de copeaux osseux autogènes. Ce mélange est effectué dans du plasma obtenu après centrifugation du sang du patient et additionné de métronidazole.
Les micro cratères obtenus avec le rayonnement du laser Er YAG provoquent également des ondes de choc à l’intérieur du site osseux receveur tout à fait favorables à une stimulation de la cicatrisation osseuse :
Apparition de mini hématomes avec apport de plaquettes et de facteurs de croissance suivi d’un tissu de granulation vascularisé qui permet la venue des CSM responsables, après leur différenciation, du premier tissu ostéoïde formé
Revascularisation accélérée avec ré oxygénation du site greffé et prolifération des ostéoblastes remplaçant progressivement le tissu ostéoide en os fibrillaire. (Monnet- Corti et coll 2006)
Le laser Er YAG (2940 nm) utilisé pour le cas clinique suivant est l’Er YAG « Pluser », de fabrication européenne (Lambda) et largement utilisé en médecine depuis de nombreuses années (fig.14).
Fig.14 – Diode « Wiser » (980 nm) et Er YAG « Pluser » (2940 nm), 2 Lasers complémentaires et utiles en chirurgie dentaire
V. A PROPOS D’UN CAS CLINIQUE
A. DIAGNOSTIC ET PLAN DE TRAITEMENT
Le patient de 62 ans est victime d’un déchaussement généralisé qui évolue depuis de nombreuses années. Cette résorption osseuse est responsable de la perte de plusieurs molaires malgré les tentatives de contention effectuée à l’aide de prothèses fixes.
L’ensemble des dents a une mobilité supérieure à 3 (sur une échelle de 4) avec un aspect clinique gingival extrêmement dégradé consécutivement aux abcès parodontaux dont le patient est victime. (Rey G, Missika P, 2010)
L’examen radiographique confirme la nécessité d’extractions complémentaires au niveau mandibulaire droit et au niveau maxillaire gauche.
Le bloc incisivo canin est d’un avenir très incertain mais le patient souhaite conserver provisoirement les dents naturelles antérieures malgré les risques réels dont nous l’informons lors de la 1° consultation. (fig.15.16.17)
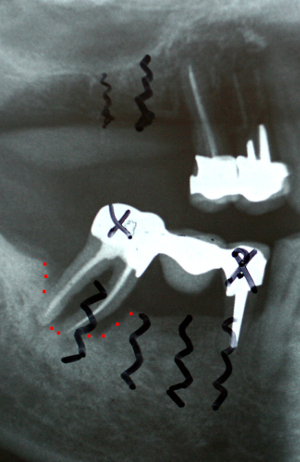
Fig.15 - Les lésions mandibulaires droites nécessitent
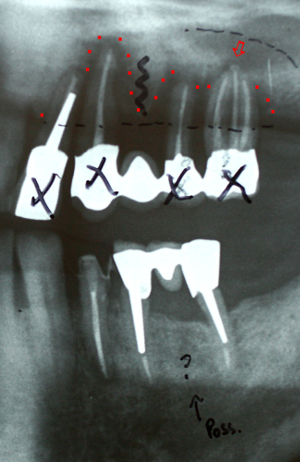
Fig.16 – L’os parodontal est inexistant au maxillaire gauche l’extraction de 25 et 27
Fig.17 - Clinique initiale, importante résorption osseuse au niveau postérieur
Une étude tomographique complémentaire par coupes transaxiales Newtom (fig.18) confirme l’existence de lésions très profondes particulièrement au niveau de la molaire 47 et du maxillaire gauche (dents 22.23.25.26) avec une communication bucco sinusienne à l’apex de la racine palatine de la molaire n°26. A ce niveau, la muqueuse du sinus est nettement inflammatoire sans signe de sinusite aigüe.
L’étude bactériologique par sonde ADN montre la présence du complexe rouge de Socransky en quantité importante, ce qui nécessite avant toute chirurgie une décontamination parodontale de toute la cavité bucco dentaire.
L’effet décontaminant du protocole de traitement parodontal laser assisté (Alpha Omega News n°148 – avril 2012) permet une décontamination immédiate, il est donc possible d’envisager l’ensemble du traitement parodontal, chirurgical et implantaire en une seule intervention.
Le plan de traitement prévoit :
1) Un traitement parodontal décontaminant conforme au protocole lasers assisté défini dans le n° 43 de la L.S. de septembre 2009
2) Les extractions des dents mandibulaires 45 et 47 et des dents maxillaires 22.23.25.26.
3) La mise en place de 6 implants type Branemark dont 2 sont placés au niveau maxillaire droit, 3 au niveau mandibulaire droit (complétés par une régénération osseuse après curetage et décontamination de la lésion existante) et un seul au niveau maxillaire gauche étant donné le peu de volume osseux résiduel sur ce site
4) Une chirurgie pré implantaire par correction du volume osseux maxillaire et mandibulaire afin d’obtenir un volume et un niveau crestal compatibles avec une prothèse fixe esthétique et fonctionnelle.
5) Le sinus gauche ouvert sur la cavité bucco dentaire à la suite de l’extraction de la molaire 26 fera l’objet d’une greffe par voie latérale (sinus lift) complété par une fermeture par voie crestale après décontamination sinusienne et préparation des corticales osseuses
B. INTERVENTION ET PROTOCLE CHIRURGICAL
Le plan de traitement chirurgical décidé en une seule intervention est effectué en milieu hospitalier sous anesthésie générale mais peut être envisagé au cabinet en plusieurs séances.
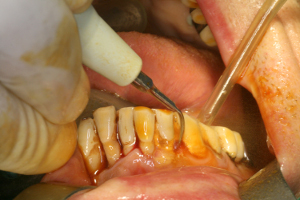
Le traitement parodontal décontaminant initial commence par un débridement de toutes les poches parodontales sous polyvidone iodée (fig.19)
Fig.19 – Traitement parodontal préparatoire
Ce débridement est effectué directement jusqu’ au contact osseux tangentiellement aux racines dentaires grâce à des inserts ultrasoniques fins utilisés avec leurs parties arrondies pour respecter au maximum le cément radiculaire.
Un détartrage minutieux plus superficiel est effectué ensuite sous eau stérile afin de permettre conjointement le rinçage de tout le système ultrasonique.
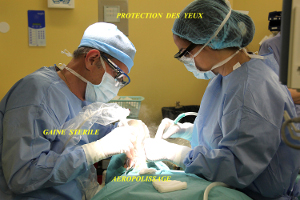
Toute cette action ultrasonique provoque une boue cémentaire qui obstrue les tubulis dentinaires, il est nécessaire de rouvrir ces tubulis dentinaires en effectuant un aéropolissage minutieux qui ôte la smear layer des surfaces radiculaires. Cet aéropolissage nécessite une protection des yeux de la part des opérateurs (fig20)
Fig.20 - Aéropolissage final pour la préparation initiale
La préparation initiale étant terminée, l’ensemble des poches parodontales est oxygéné par un dépôt de peroxyde d’hydrogène à 3 % laissé plusieurs minutes pour permettre une oxygénation des tissus en profondeur.
Pendant ce temps, le laser diode est préparé avec une gaine stérile et une fibre de 400 µ. Les réglages sont choisis en fonction de l’étude bactériologique initiale et de la profondeur des poches parodontales, il est ici de 2,5 w avec un Ton de 50 µs et un Toff de 117 µs ce qui permet d’obtenir une puissance moyenne de 0,7 w et une fréquence de 6000 Hz.
Ces différents réglages sont aujourd’hui directement accessibles sur le laser Wiser avec une possibilité de modification en cas de nécessité.
Un avantage des lasers diodes est leur miniaturisation qui permet très facilement de les transporter au bloc opératoire et de les utiliser avec la protection d’une gaine stérile (fig.21)
Fig.21 - Le laser est équipé d’une gaine stérile
Le rayonnement laser est actionné dans toutes les poches parodontales jusqu’au contact osseux par des mouvements de va et vient, soit en direction du cément radiculaire soit en direction de la gencive périphérique.
Les réglages décontaminants disponibles sur le Wiser n’occasionnent que des effets thermiques de vasodilatation, il est donc possible d’effectuer cette action très rapidement sans temps de repos. (fig.22)
IMPORTANT : pour cet effet photo dynamique décontaminant, il faut que la fibre optique du laser ne soit pas carbonisée à son extrémité, sinon la carbonisation bloque le rayonnement qui ne pénétrerait plus en occasionnant des effets thermiques superficiels. En cas de carbonisation, la fibre doit être nettoyée, coupée ou changée.
Fig.22 - Décontamination laser assistée au maxillaire
De l’eau oxygénée peut être replacée au fur et à mesure si nécessaire à condition que l’assistante aspire les excès dans la cavité bucco dentaire
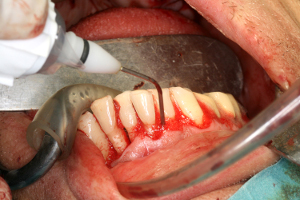
Tous les tissus parodontaux et dentaires sont méthodiquement décontaminés aussi bien sur les faces vestibulaires que sur les faces linguales ou palatines des deux maxillaires (fig 23)
Fig.23 - Décontamination laser assistée à la mandibule
Le traitement parodontal préparatoire étant terminé, l’implantologie et la chirurgie de reconstruction osseuse peuvent être envisagées
2. IMPLANTOLOGIE ET CHIRURGIE RECONSTRUCTRICE
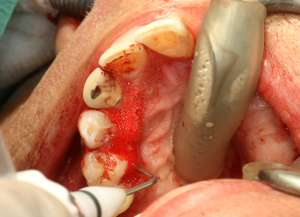
Les lambeaux d’accès aux volumes osseux résiduels sont pratiqués à ce moment après la chirurgie parodontale.
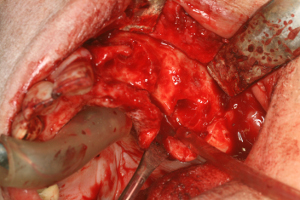
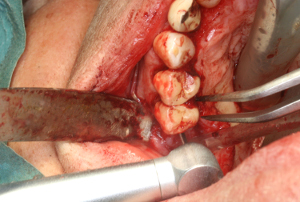
Ces lambeaux permettent de découvrir des lésions osseuses extrêmement profondes à la mandibule et au niveau du maxillaire gauche (fig 24)
Toutes ces lésions font l’objet d’un curetage minutieux suivi d’une décontamination des volumes osseux effectuée avec le laser Diode sous peroxyde d’hydrogène à 3 % directement au contact des surfaces osseuses (puissance 2,5 w et augmentation du temps de repos à 80 % de la période).
Le sinus gauche fait également l’objet de la même action décontaminante par la communication existante au niveau de la dent 26 en réduisant la puissance du laser « Wiser » à 2 w avec un temps de pulse de 20 % de la période.
Fig.24 – Absence totale de l’os parodontal au maxillaire gauche
Il est nécessaire de favoriser les échanges entre l’os autogène du patient et les biomatériaux déposés dans le but d’obtenir une reconstruction du volume osseux. Ceci est réalisé avec l’Er YAG qui permet une décorticalisation superficielle avec apparition de micro cratères.
Les réglages choisis pour décorticaliser les surfaces osseuses dépendent de la qualité de l’os rencontré et sont ici de 200 mj à 20 Hz au maxillaire et de 230 mj à 30 Hz à la mandibule. (fig.25)
Fig.25 – Protection stérile du laser Er YAG
Dans les deux cas, c’est un tips de 600 µ de diamètre qui est choisi.
Le spray d’air et d’eau est également réglable sur ce laser. Nous utilisons 70 % d’air et 80 % d’eau.
Toutes les lésions et toutes les corticales osseuses sont ainsi préparées avec le laser 2940 nm avant tout forage implantaire. (fig.26)
Fig.26 - Préparation des corticales osseuses au Laser Er YAG
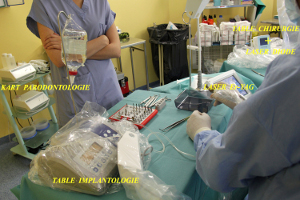
C’est seulement après cette préparation initiale que la table d’implantologie est avancée par l’infirmière à coté du laser Erbium et du laser Diode qui peuvent ainsi être ré-utilisés en cas de nécessité. (fig.27)
Fig.27 – Organisation du bloc opératoire
Dans le cas de ce patient, nous mettons en place six implants Nobel de type Branemark dans les volumes osseux résiduels (3 à la mandibule secteur droit et 3 au maxillaire)
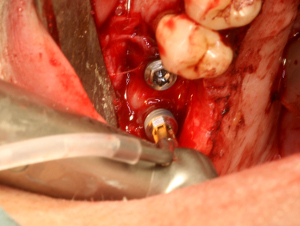
Les implants sont placés au contre angle avec un tour réglé sur un torque de 25 newtons, la mise en place finale se faisant grâce à la clé dynamométrique. (fig.28)
FIG.28 – Mise en place des implants Nobel
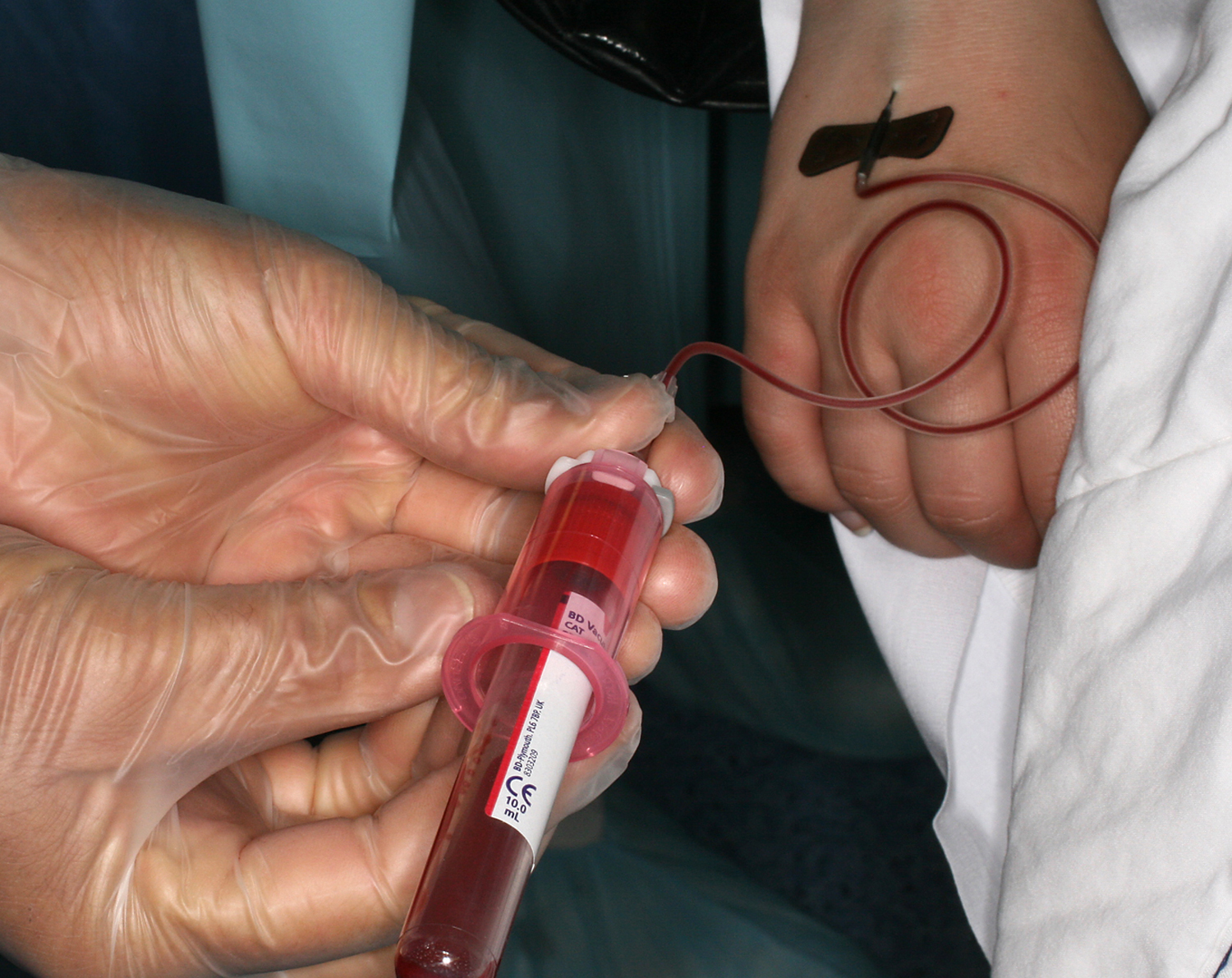
Pendant cette phase d’implantologie, le sang du patient est prélevé (fig.29) et centrifugé à 3000 tours pendant 11 minutes dans le but d’obtenir des caillots de fibrine riche en plaquettes (PRF) qui contiennent les facteurs de croissance que nous souhaitons mélanger à la xénogreffe. (Mole C. 2006)
Fig.29 – Prélèvement sanguin pour centrifugation
Dans certains cas, ces caillots de fibrine riches en plaquettes peuvent contenir, dans leur partie inférieure, des cellules souches (ceci n’est pas systématique). C’est pour cette raison que nous séparons le culot des caillots pour les mélanger au Bio-oss granules fins.
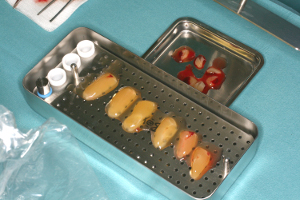
Le reste des caillots est déposé dans la PRF box afin d’ obtenir des membranes PRF que nous utilisons pour le maintien initial des biomatériaux avec l’avantage de recueillir également des facteurs de croissance et des cytokines favorables à la première cicatrisation (fig.30) (Choukroun 2001)
Fig.30 – La PRF Box permet la récupération du plasma
Les culots des caillots finement découpés sont mélangés au Bio-oss et au plasma obtenu dans la PRF Box
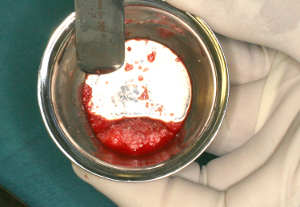
Nous prélevons également dans les sites de forage un volume de copeaux osseux le plus important possible que nous mélangeons à notre biomatériau. (fig.31) (Rey G et coll 2008)
Fig.31 – Obtention d’un mélange compact et facilement malléable de Bio-oss + PRF + Copeaux osseux
Après addition de métrodinazole, l’excès de liquide est aspiré afin d’obtenir un mélange que nous souhaitons légèrement compact pour tenir sur les sites receveurs, mais encore très malléable pour pouvoir être déposé dans toutes les anfractuosités et comprimé délicatement sans pression excessive
C. RESULTATS CLINIQUES ET RADIOGRAPHIQUES ……..
Les résultats cliniques obtenus immédiatement semblent toujours assez inquiétants pour les grandes reconstructions osseuses.
L’anatomie est toujours chaotique et les membranes collagènes dénudées laissent apparaitre une fibrine non vascularisée dont il faut aider la transformation en épithélium vascularisé. Les lasers Diodes sont ici d’une grande utilité.
La technique est très simple mais doit être rigoureusement mise en œuvre pour améliorer l’anatomie osseuse et gingivale nécessaire à l’implantologie prévue ultérieurement.
Le patient est revu au minimum chaque semaine jusqu’à la fermeture de la plaie initiale.
La plaie est oxygénée par dépôt d’eau oxygénée à 10 volumes sous les berges et directement sur la fibrine visible.
Le laser Diode Wiser est directement réglé en photothérapie dynamique faible ou moyenne (ici, 2 w avec un Ton de 25 % de la période et une fréquence de 3000 à 5000 Hz environ)
Avec ce réglage, la fibre de 400 µ est mise en contact avec la fibrine et passée sous les berges pour obtenir une action thermique de vasodilatation et un effet de photothérapie dynamique destiné à éviter toute recontamination du greffon.
Le contact de la fibre de 400 µ sous les berges et l’effet thermique provoquent un saignement qui doit être le plus abondant possible pour recouvrir totalement la plaie existante initialement.
Tout ce protocole est très facilement applicable sans anesthésie, il est totalement indolore.
Le caillot sanguin obtenu est laissé en place sans aucun rinçage postopératoire.
Pour terminer, une biostimulation avec la lentille défocalisante est effectuée sur l’ensemble du site (Réglage entre 2 et 3 w en continu, mais en déplacement constant pour maitriser l’effet thermique à 45 ou 50 ° maximum).
NOTE : Nos recherches les plus récentes sur les effets biostimulants des rayonnements lasers pénétrants nous conduisent à abandonner le mode continu au profit d’un réglage en microsecondes (µs) permettant une fréquence super pulsée de plusieurs KHz (entre 8000 Hz et 15000 Hz) afin d’augmenter l’énergie des photons (constante de Planck X fréquence).
La puissance est augmentée entre 6 et 7 watts avec un réglage des temps de repos (Toff) de 70 % de la période qui permet d’obtenir une puissance moyenne d’environ 2 watts.
Ce réglage est modulé en fonction des tissus cibles dans le but de limiter l’effet thermique à la vasodilatation souhaitée.
L’utilisation de la lentille défocalisante est ainsi nettement facilitée même en postopératoire sur des tissus anesthésiés.
Le caillot sanguin étant laissé en place et la biostimulation terminée, la pothèse transitoire est aussitôt replacée en ayant pris la précaution de parfaitement creuser et arrondir l’intrado au niveau crestal pour maintenir le caillot sanguin formé sans le comprimer.
Il est demandé au patient de ne pas enlever la prothèse amovible jusqu’au lendemain matin et d’effectuer son hygiène bucco dentaire avec la prothèse en place. Les jours suivants, il devra respecter une hygiène bucco dentaire douce et ne pas toucher le site d’intervention.
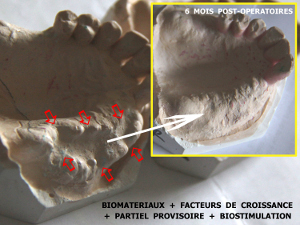
Les résultats permettent toujours d’obtenir une très bonne amélioration de l’anatomie crestale et dans le cas de ce patient, l’étude comparative des modèles postopératoires et à 6 mois (fig.36) permet de constater la bonne transformation de la crête maxillaire gauche.
Fig.36 – Résultat d’un greffon biostimulé et soutenu par une prothèse amovible stable
Une radiographie panoramique de contrôle est effectuée à 6 mois postopératoires (fig.37) et permet de constater la bonne ostéo intégration des implants Nobel Branemark avec une bonne restructuration des greffons qui montre déjà une résorption des biomatériaux avec une première transformation du tissu ostéoïde en os minéralisé. (Monnet-Corti, Roche-Poggi, 2006)
Fig.37 – Contrôle à 6 mois postopératoires
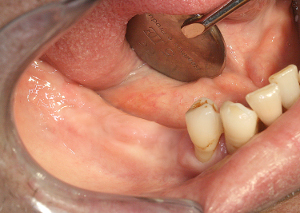
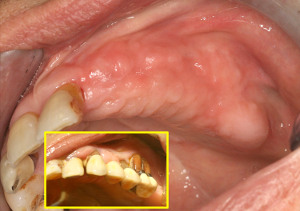
L’état clinique mandibulaire est également satisfaisant (fig.38).
Fig.38 - Etat clinique mandibulaire de la crête greffée.
Fig.39 Mise en place d’une prothèse mandibulaire implanto portée
La prothèse mandibulaire implanto portée de 3 éléments est placée en respectant la courbe de Spee.
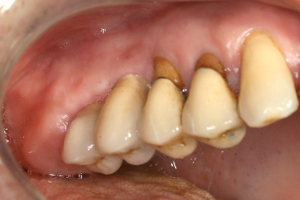
Pour le maxillaire droit, l’épaisseur gingivale très importante au niveau des molaires (fig.40) est nettement diminuée à la mise en place des vis transgingivales de cicatrisation, grâce à l’action ablative du laser Er YAG sur les tissus mous (réglages : 160 mj à 30 Hz avec un tips de 600 µ) (fig.41)
Fig.40- Epaisseur gingivale trop importante au maxillaire droit
Fig.41 -Effet ablatif du laser Er YAG « Pluser » sur les tissus gingivaux
Cette ablation des tissus gingivaux (Rocca JP et coll 2008) permet de retrouver une crête compatible avec une prothèse implanto portée fonctionnelle et avec l’hygiène bucco dentaire quotidienne (fig.42).
Fig.42 – Mise en place du bridge implanto porté au maxillaire droit
A 6 mois postopératoires, des coupes tomographiques de contrôle sont demandées au niveau du maxillaire gauche (coupes Newtom) pour vérifier l’intégration des greffes crestales et sinusiennes effectuées. (Maujean E, Struilloux, 2004)
Ces coupes mettent en évidence un nouveau volume osseux en cours de transformation largement suffisant pour la mise en place d’implants dentaires (fig.43).
Nous constatons également la guérison de la pathologie sinusienne suite à la décontamination laser assistée effectuée conjointement au sinus lift et à la greffe crestale (fig. 44)
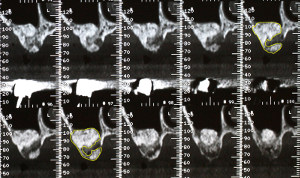
Fig.43 – Vérification tomographiques par coupes transaxiales
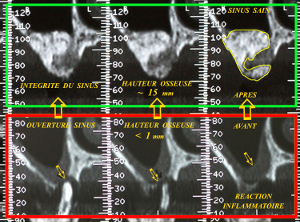
Fig.44 – Comparaison sur coupes transaxiales avant et après traitement
Les coupes tomographiques tangentielles au niveau de l’ouverture bucco sinusienne initiale montrent le nouveau volume osseux reconstitué par le greffon crestal et par la greffe intrasinusienne (fig.45)
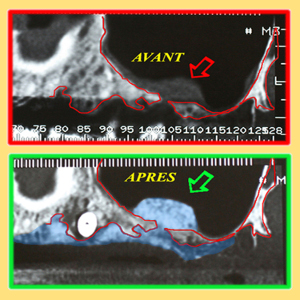
Fig.45 – Coupes tomographiques tangentielles avant et après chirurgie pré implantaire laser assistée
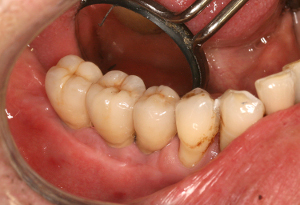
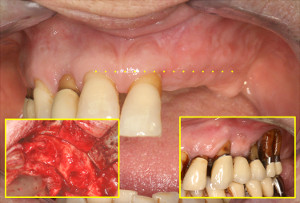
L’état clinique obtenu (fig.46) confirme que le niveau crestal gingival est aujourd’hui identique du coté droit et du coté gauche. L’augmentation de hauteur visible est supérieure à 15 mm au niveau de la molaire 26.
Fig.46 – Résultat clinique de la hauteur de crête obtenue
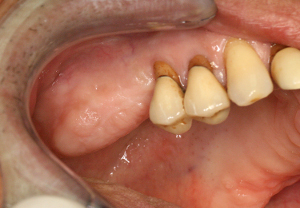
L’épaisseur de cette crête qui était initialement très faible au niveau des dents 22.23 et 25 est également nettement améliorée cliniquement (fig.47).
Fig.47 – Résultat clinique de l’épaisseur de crête obtenue
Cet état clinique est confirmé à la mise en place des implants complémentaires qui est effectuée à 8 mois postopératoires (fig.48)
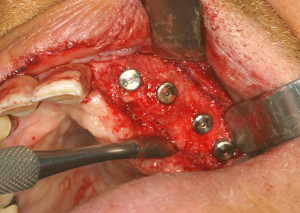
Fig.48 – L’implantologie peut être pratiquée sur une crête large et dense
Le volume osseux et la largeur de la nouvelle crête osseuse permettent la mise en place de 3 implants supplémentaires au même niveau crestal que l’implant placé précédemment.
La qualité de l’os obtenu à 8 mois postopératoires montre une bonne résorption du biomatériau avec le remplacement par un os naturel bien vascularisé et suffisamment compact. Les implants sont mis en place avec un torque initial de 30 newtons au minimum.
Pour une raison purement esthétique, il est prévu un bridge dento implanto porté qui réunira au choix du patient une ou plusieurs incisives avec les implants maxillaire gauche.
VI. CONCLUSIONS
Ce protocole laser assisté qui définit une parfaite décontamination avant toute chirurgie peut être également utilisé pour tout type de chirurgie et pour tout type de greffes (autogreffes, xénogreffes, allogreffes, ….), cette décontamination initiale essentielle pouvant parfaitement être effectuée dans la même séance opératoire grâce à la photothérapie dynamique obtenue avec un rayonnement laser pénétrant dirigé sur des tissus cibles préalablement oxygénés.
Pour cette action prioritaire, il est nécessaire d’utiliser un rayonnement pénétrant type Diode ou Nd YAG, les diodes modernes permettant beaucoup plus facilement de maitriser l’effet thermique généré par le rayonnement laser.
L’énergie d’un photon étant proportionnelle à la fréquence du rayonnement, le réglage en mode superpulsé (5000 Hz ou plus) est également un avantage important.
La deuxième obligation est la décorticalisation des tissus osseux superficiels avec la formation de multiples micro cratères et d’ondes de choc intra osseuses qui permettent les échanges initiaux indispensables à l’intégration et à la transformation des biomatériaux.
Cet acte n’est possible qu’avec un laser Er YAG (2940 nm) ou ErCrYSGG (2780 nm) qui permettent une action sur les tissus osseux grâce au spray de refroidissement qui accompagne le rayonnement.
La troisième action des lasers dans ce protocole est la biostimulation postopératoire pour laquelle nous utilisons le laser Diode « Wiser » à rayonnement pénétrant mais que nous équipons cette fois d’une lentille défocalisante à embout courbe afin d‘accéder facilement à toutes les faces postérieures des sites d’intervention.
Ces deux longueurs d’onde (980 nm et 2940 nm) s’avèrent donc extrêmement complémentaires et tout à fait favorables à la réussite de ce type de chirurgie. (fig.49)
Fig.49 – Diode 980 nm et Er YAG 2940 nm, les 2 longueurs d’onde complémentaires de la chirurgie pré implantaire moderne
Les autres facteurs qui nous semblent importants pour la réussite de ces chirurgies pré implantaires lasers assistées sont :
Choix d’un biomatériau d’une structure proche de l’os humain (ici Bio-oss granules fins)
Adjonction de fibrine riche en plaquettes (membranes PRF + facteurs de croissance) et de copeaux osseux autogènes dans ces biomatériaux (obtention d’un mélange homogène malléable et meilleure néo vascularisation initiale)
Protection des greffons par des membranes collagènes avant fermeture
Mise en place de prothèses amovibles stables et non compressives au niveau crestal
Délai d’attente de 7 à 8 mois au minimum pour obtenir une structure osseuse néo formée suffisamment compacte et bien vascularisée favorable à l’ostéo intégration des implants envisagés.
Le respect de ce protocole permet aujourd’hui d’assurer un succès prévisible et répétitif à toutes les chirurgies pré implantaires avec l’obtention d’un nouveau volume et d’une qualité osseuse favorable aux réalisations prothétiques implanto portées qui paraissaient initialement impossibles ou très complexes.
Parution Lettre de la Stomatologie 56 - Novembre 2012
BIBLIOGRAPHIE
BERT M , MISSIKA P. Les clés du succès en implantologie. 2010 ; Ed CdP Coll JPIO
CACCIANIGA G, MONGUZZI R, REY G, MARTELLI S. Srgie entre laser et PRP dans la régénération osseuse. Alpha Omega News 2005 ; Sept. : 4-7.
CACCIANIGA GL, URSO E, MONGUZZI R, GALLO K, REY G. Effecto bactericida del laser de diodo en periodoncia. Avances en periodoncia e implantologia oral dec. 2007 ; vol. 19 N°3.
CHAVOIN JP, BRUNETAUD JM, GAILLOT-MAUGIN J, GODARD B, LECARPENTIER Y, LAFITTE F, MORDON S, ROUX FX, SULTAN R. Encyclopédie des lasers en médecine et en chirurgie. Ed. Piccin 1995.
CHOUKROUN J, ADDA F, SCHOEFFLER C, VERVELLE A. Une opportunité en paro implantologie, le PRF. Implantodontie 2001 ; 42 : 55-62.
DOHAN D, DISS A. Compte rendu du 2° symposium international sur les facteurs de croissance. Implantodontie 2005 ; 14 : 116-125
KHOURY G. Les matériaux allogéniques de substitution osseuse. Clinic 2008 ; juillet : 11-15
MAUJEAN E, STRUILLOU X. Comblement de sinus et biomatériaux : revue de littérature. JPIO 2006 ; 25 : 35-43.
MISSIKA P, STROUMZA JM. Traitement des péri impantites avec le laser Nd Yap : à propos d’un cas. Revue d’odontostomatologie sept. 2003 ; 215-229.
MOLE C. Rôle des concentrés plaquettaires dans la cicatrisation et la régénération osseuse. JPIO 2006 ; 25 : 45-62.
MONNET-CORTI, ROCHE-POGGI P. Principes biologiques mis en jeu dans la cicatrisation osseuse. JPIO 2006 ; 25 : 5-13.
REY G. L’apport du laser dans le traitement des poches parodontales. Implantodontie sept.2000 ; 27-34.
REY G. L’apport du laser dans les parodontites et les peri implantites. La lettre de la stomatologie 2001 ; avril : 6-9.
REY G. Protocole de traitement parodontal lasers assisté. Alpha Omega News 2012 ; 148 : 21-23
REY G, CACCIANIGA G. La régénération osseuse et les lasers en Odontostomatologie. Alpha Omega News 2010 ; 131 : 16-19
REY G, CACCIANIGA G, GOUVERNET M. Lasers + Biomatériaux + PRF. La lettre de la Stomatologie 2010 ; 48 : 4-33
REY G, FROMENTAL R, CACCIANIGA GL, et al. Lasers et implantologie, les raisons d’un mariage incontournable. Implantologie 2008 ; nov. : 39-56
REY G, MISSIKA P et col. Les lasers et la Chirurgie dentaire. 2010 ; Ed CdP col JPIO
REY G, MISSIKA P. Traitements parodontaux et lasers en omnipratique. 2010 ; Ed Elsevier Masson
REY G, MISSIKA P. Lasers et Implantologie. Information dentaire 2010 ; 16 : 21-29 - 17 : 12-17
ROCCA JP. Les lasers en odontostomatologie – Memento Editions CDP. 2008