Action des lasers diode sur les Staphylococcus Auréus
 Etudes in vitro et résultats
Etudes in vitro et résultats
Mis au band d'essai les différents lasers...
Docteur Gérard REY
Diplômé de la Faculté de Médecine
Directeur de l’Enseignement des Lasers Médicaux
Paris 7 Garancière – Milan Bicocca – Montpellier UFR
ACTION DES LASERS DIODES SUR STAPHYLOCOCCUS AUREUS ETUDES IN VITRO ET RÉSULTATS
-
INTRODUCTION
Les traitements lasers assistés font partie des données acquises de la science médicale et l’historique de toutes les recherches cliniques effectuées depuis presque 30 années est longuement décrit dans le N°76 de la « Lettre de la Stomatologie » (page 6 à 33).
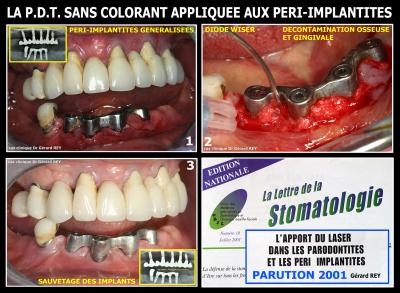
De nombreuses vérifications de la décontamination obtenue avec le protocole « PDT sans colorant » ont été faites conjointement par les Universités de Paris Garancière et Milan Bicocca qui furent innovatrices dans ce domaine en introduisant l’enseignement des techniques lasers assistées depuis le début des années 2000.

Fig.1 – Une collaboration Européenne interuniversitaire
Cette alternative de soins s’est imposée dans l’arsenal thérapeutique de l’ensemble de notre profession, particulièrement en raison des propriétés biostimulantes et décontaminantes qui constituent un acte de prévention utile dans de nombreux domaines de l’Odontostomatologie.
-
HISTORIQUE ET PREMIÈRES ÉTUDES IN VITRO
Au cours des années 90, les applications cliniques étaient réalisées grâce aux parutions cliniques disponibles à l’époque :
-
Université de Tokyo 1996 « Clinical efficacy of the Nd :YAG laser for combination periodontis therapy » (Ando Y, Aoki A et col. 1996)
-
Université de Vienne 1998 « Treatment of periodontal pockets with a diode laser » (Moritz A, Gutnetch N et col. 1997)
L’ensemble de ces parutions indiquaient que le rayonnement laser avait un pouvoir bactéricide sur les bactéries pathogènes parodontales avec différentes longueurs d’onde.
Les résultats cliniques obtenus furent très décevants, le rayonnement laser utilisé seul ne permettant aucun effet bactéricide, en dehors d’une action thermique très forte peu souhaitable dans l’objectif de conservation des tissus sains.
De la même façon, l’addition de colorants avant le rayonnement laser (PDT utilisée en dermatologie sur les mélanomes) ne donnait pas non plus un bon résultat décontaminant, le colorant bloquant la pénétration du rayonnement dans la profondeur des tissus infectés.
Le remplacement du colorant par du Peroxyde d’Hydrogène à 3 % a permis immédiatement de bons résultats cliniques dans les thérapeutiques parodontales ou péri-implantaires en provoquant des réactions de photo-oxydation et la production d’oxygène singulet puissamment bactéricide.
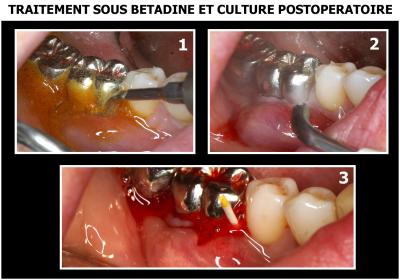
En 2001, ces résultats décontaminants ont été confirmés par une 1ère étude in vitro réalisée en collaboration avec l’Institut Biomatech et l’Institut Pasteur (fig. 2)

Fig. 2 – 1ères études in vitro du protocole « PDT sans colorant » élaboré par G. REY - Montpellier
Cette étude est réalisée avec une longueur d’onde de 1340 nm dont l’effet thermique important nécessite une prudence dans les temps d’irradiation qui ne peuvent pas dépasser quelques secondes (avec des temps de repos intermédiaires).
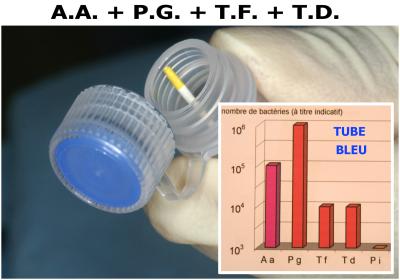
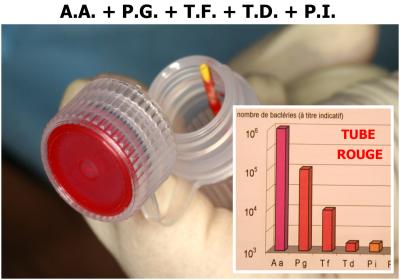
Les études réalisées ont démontré que seule une bactérie (Aggregatibacter Actynomicetemcomitans) est sensible au Peroxyde d’Hydrogène et au rayonnement laser, l’ensemble des autres pathogènes nécessite l’oxygénation préalable des tissus infectés pour obtenir une bonne décontamination lors de l’irradiation par le rayonnement laser : tests sur Bactéroides forsythus (Tannarella forsythia), Porphyromonas gingivalis, Micromonas micros (Petostreptococcus micros) et Fusobacterium nucleatum. (fig. 3)
Fig. 3 – Les résultats obtenus permettent de valider le protocole « Peroxyde d’hydrogène + Laser »
D’autres études sont menées par la suite avec d’autres longueurs d’onde :
Plusieurs tests sont effectués avec des lasers Diode en 2002, 2003 et 2004 dont une étude avec l’Institut Pierre Fournier à Paris sur trois pathogènes parodontaux (Prevotella intermedia, Peptostreptococcus micros, Fusobacterium nucleatum) qui confirme les bons résultats du protocole « Peroxyde d’Hydrogène + laser ».
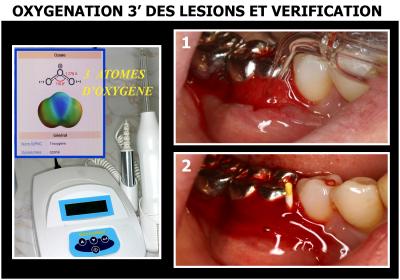
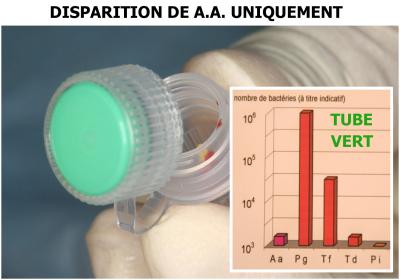
Les réglages d’un laser Diode permettent une durée d’irradiation plus importante grâce à une bonne maitrise des effets thermiques, les résultats obtenus montrent une excellente diminution bactérienne jusqu’à 99 ,999 et même 100 %. (fig. 4 et 5).

Fig. 4 – Etudes avec longueur d’onde 980 nm à Fig. 5 – Conclusions de l’étude de 2004 sur l’effet
L’Institut Pierre Fournier (2004) par les Docteurs décontaminant des lasers Diode sous H2O2
G.REY et P. SEDNAOUI
Les différentes vérifications effectuées ont permis un récapitulatif précis qui démontre que :
-
Seule Aggregatibacter actynomicetemcomitans est sensible au rayonnement laser
-
Seules Aggregatibacter actynomicetemcomitans et Prevotella intermedia sont sensibles au Peroxyde d’hydrogène
-
L’ensemble des bactéries parodonto-pathogènes sont sensibles au protocole « Peroxyde d’Hydrogène + Laser » (fig. 6)
Les premières parutions sur l’effet décontaminant de cette PDT sans colorant datent de 2000 dans la revue « Implantodontie » (n°38) et de 2001 dans la revue N°10 de « La Lettre de la Stomatologie ». (Rey G. 2000) (Rey G. 2001).

Fig. 6 – Conclusions sur l’effet bactéricide des différents tests effectués
-
APPLICATIONS CLINIQUES EN ODONTOSTOMATOLOGIE
Dans le domaine de l’Odontostomatologie, les applications cliniques permettent de rapides et nombreuses guérisons des infections parodontales et péri-implantaires sans antibiothérapie dans la grande majorité des cas.
Exemple de traitement parodontal à visée conservatrice
Le patient de la figure 6 est victime d’une parodontite agressive avec de nombreuses poches maxillaires et mandibulaires.
L’étude bactériologique montre de nombreuses bactéries pathogènes en grande quantité (Aggregatibacter actynomicetemcomitans, Porphyromonas gingivalis, Prevotella intermedia, Bacteroides forsythus, Peptostreptococcus micros, Fusobacterium nucleatum, Treponema denticola).
Le plan de traitement envisagé est initialement, l’extraction de 9 dents déchaussées et mobiles, complété par la mise en place de 6 ou 7 implants et la réalisation d’une prothèse implanto-portée (fig. 7)

Fig. 7 – Etat initial du patient B (radiographique et bactériologique)
Le traitement laser assisté ne comprend qu’une préparation parodontale rigoureuse (débridement, détartrage et surfaçage radiculaire, aéropolissage, suivis de l’effet décontaminant obtenu avec un laser Diode sous Peroxyde d’Hydrogène). (Rey G, Missika P. 2010).
Ce traitement décontaminant laser assisté permet d’obtenir la disparition des bactéries pathogènes et en conséquence, la cicatrisation des tissus gingivaux et osseux, sous réserve d’une hygiène buccodentaire adaptée à ce cas particulier (Fig. 9) (Caccianiga GL et col. 2007).


Fig. 8 – Etat clinique du patient B (présence de Fig. 9 – Etat clinique du patient B après traitement
7 pathogènes parodontaux en grande quantité décontaminant lasers assisté. L’étude
bactériologique montre l’absence totale de
bactéries parodonto-pathogènes
Ce patient, pour des raisons esthétiques, demande la réalisation d’un bridge céramo-métallique qui n’est réalisé qu’après la cicatrisation gingivale et osseuse (vérification radiographique indispensable) (fig. 10)
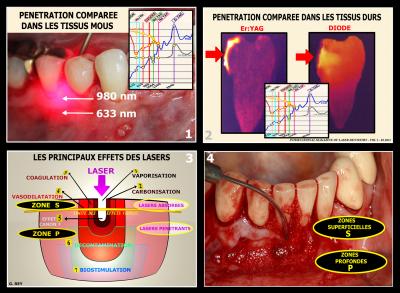
Fig. 10 - Réalisation d’un bridge d’usage après la cicatrisation gingivale et osseuse
Exemple d’un cas chirurgical à visée reconstructrice
Cette technique de décontamination par PDT sans colorant a de nombreuses applications dans le domaine chirurgical, particulièrement en Implantologie et en Chirurgie reconstructrice.
Elle augmente nettement le taux de succès en Implantologie post-extractionnelle immédiate et elle permet de décontaminer les sites osseux receveur avant toute greffe ou régénération osseuse guidée. En complément, la biostimulation entraine une respiration cellulaire et une synthèse de l’ATP favorable à la cicatrisation des tissus.
Il est possible d’effectuer conjointement à des extractions, une décontamination des tissus osseux et même une décontamination intra-sinusienne, ce qui permet, dans la même séance, une chirurgie implantaire complétée par une greffe crestale et un sinus-lift (fig. 11) (Rey G. 2009, 2010,2017).

Fig. 11 – Exemple d’une chirurgie complexe effectuée en une séance grâce à l’aide des lasers
-
AUTRES APPLICATIONS MÉDICALES
Depuis 2011 et 2012, différentes spécialités médicales se sont penchées sur l’utilisation de cette « Photothérapie Dynamique sans colorant » afin de
décontaminer les plaies ou les sites chirurgicaux infectés sans l’apport des antibiotiques.
Les résultats obtenus avec un laser diode réglé sur une Fréquence élevée et un apport cyclique permettant une bonne maitrise des effets thermiques associés sont souvent exceptionnels avec une guérison rapide des plaies infectées qui sont d’abord nettoyées puis oxygénées au Peroxyde d’Hydrogène à 3 % avant d’être exposées à l’irradiation du rayonnement laser.
Exemple de l’infection d’un doigt
Il s’agit d’une infection post-chirurgicale d’un index avec un aspect nécrotique de la plaie alarmant malgré l’antibiothérapie.
Cette plaie est nettoyée et oxygénée avant de subir une irradiation laser avec un laser Diode de 980 nm, réglé sur : P Crête : 2,5 w – 6000 Hz – P moyenne 0,7 w.
Deux séances de « PDT sans colorant » suffisent à refermer la plaie et deux autres séances de biostimulation (au laser Diode et ATP 38) permettent de retrouver une fermeture totale avec une cicatrisation correcte des tissus initialement infectés et nécrosés. (Fig. 12)

Fig. 12 – Exemple de la guérison d’une plaie infectée grâce à 2 séances de décontamination
et 2 séances de biostimulation
-
COLLABORATION ENTRE PROFESSIONNELS DE SANTÉ
En 2016, les Docteurs Pierre BONNIN et Jean-Pierre BRU m’invitent à une présentation au Centre Hospitalier d’Annecy afin de leur indiquer les protocoles utilisés en Odontostomatologie, les indications thérapeutiques et l’historique des tests de laboratoires effectués.
Je réponds volontiers à cette invitation lors d’un déplacement à l’Université de Genève, et pendant deux heures, je réponds aux questions de mes confrères à l’aide d’un diaporama expliquant les plans de traitement et les résultats obtenus dans notre domaine professionnel.
Ces médecins spécialisés en Infectiologie et Endocrinologie sont préoccupés par les bactéries multi résistantes telles que les entérocoques résistants à la Vancomycine et entérobactéries résistantes aux Céphalosporines de 2ème génération …
La destruction d’une bactérie particulièrement tenace les intéresse au plus haut point : Staphylococcus Aureus : cette bactérie Gram + est résistante à la Métycilline et résistante aux Glycopeptides.
Elle pose de nombreux problèmes dans les infections des malades diabétiques et particulièrement dans les ostéonécroses des « pieds diabétiques » qui sont des affections difficiles à traiter avec des rémanences bactériennes importantes expliquant souvent les échecs qui peuvent entrainer une morbi-mortalité importante (fig. 13)
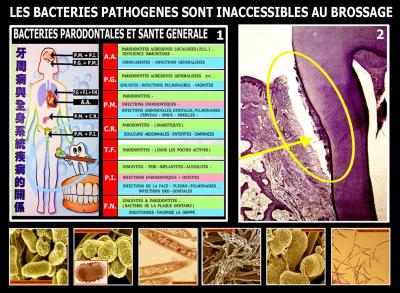
Fig. 13 – Les ostéonécroses des « pieds diabétiques » sont une pathologie très délicate à traiter
Le fait que Staphylococcus Aureus soit une bactérie aérobie donne peu d’espoir d’obtenir un effet bactéricide satisfaisant par l’apparition de l’oxygène singulet obtenue dans le protocole « PDT sans colorant ».
Il est cependant décidé d’effectuer les recherches nécessaires pour confirmer ou non l’efficacité de ce traitement laser sur « Staphylococcus Aureus ».
Le Docteur Pierre BONNIN élabore un projet de protocole qui prévoit une collaboration entre différents services hospitalo-universitaires (Paris, Annecy, Nantes, …) et particulièrement les études in vitro nécessaires sur modèles animaliers, prévues avec le groupe hospitalo-universitaire Paris Ile de France Ouest dont la première partie doit avoir lieu entre l’Hôpital Raymond Poincaré de Garches et les services de recherches de l’Ecole Nationale vétérinaire d’Alfort (E.N.V.A.)
Tout ceci nécessite un budget très important que nous parvenons à réunir ensemble avec le Docteur Pierre BONNIN.
Pour ma part, je solliciterai l’ensemble des fabricants de lasers, les seuls ayant accepté de nous aider sont :
-
Biotech Inernational
-
Swiss Bio Inov
-
Lambda SpA.
Je demande également une aide logistique à la Société Kaelux pour le transport et l’installation des différents lasers indispensables, demande qui est immédiatement acceptée par Kaelux.
Que tous ces sponsors soient remerciés, sans eux ces recherches médicales importantes n’auraient pas été possibles.
Les problèmes administratifs étant très lourds à maitriser dans le domaine médical, je décide d’alerter les Ministères concernés dans le but de mettre en place une recherche européenne menée conjointement entre plusieurs universités.
Le Cabinet du Premier Ministre répond très favorablement le 15 septembre 2017, puis le 23 février 2018 en nous assurant « qu’ils ont pris bonne note des attentes que nous formulons sur la prévention et l’innovation médicale qui représentent un enjeu de santé publique majeure en France ».
Le Cabinet du Premier Ministre transmet l’ensemble du dossier à Madame la Ministre des Solidarités et de la Santé. Nous sommes reçus à plusieurs reprises au Ministère des Solidarités et de la Santé par les chargés de mission. Ceux-ci n’ont pas souhaité encombré leur emploi du temps avec nos volumineux dossiers et n’ont manifesté qu’un intérêt très relatif pour les vidéos de présentation que nous avions longuement préparées afin de les tenir informés des 20 années de recherches universitaires qui précédaient notre visite dans leurs bureaux ….
Nous avons donc décidé d’agir seuls avec l’aide des industriels et des scientifiques américains et chinois, beaucoup plus intéressés par nos résultats que nos interlocuteurs du Ministère de la Santé … Des délégations des U.S.A. et de Chine étant venues spécialement à Paris pour proposer une collaboration scientifique et technique.
Fig. 14 et 15 – Visite des délégations chinoises et américaines à la Faculté de Paris Garancière
Voilà de quoi encourager des chercheurs français bénévoles à exporter leurs travaux vers des pays lointains…
Par sécurité, nous décidons, avant les études in vivo sur modèles animaliers, d’effectuer une première étude in vitro afin de déterminer avec exactitude les réglages des lasers et l’action éventuelle de la « PDT sans colorant » sur le germe « Staphylococcus Aureus ».
Les lasers Diodes ayant une bonne pénétration et permettant un réglage précis pour maitriser les effets thermiques, il est décidé d’effectuer ces tests in vitro avec des lasers Diodes.
Cinq lasers sont proposés pour ces tests (Fig. 16)
-
Laser Diode Epic Pro de 980 nm
-
Laser Diode Epic X de 940 nm
-
Laser Diode Wiser Icône de 980 nm
-
Laser Sirolase Blue de double longueur d’onde 445 nm + 970 nm
-
Laser Diode Piion de double longueur d’onde de 470 nm + 980 nm
Il est impératif pour nos tests que nous puissions maitriser avec une grande précision les effets thermiques des différents rayonnements lasers et nous devons également tester différentes longueurs d’onde (ou l’addition de 2 longueurs d’onde différentes) afin de constater si le choix d’une ou plusieurs longueurs d’onde a une importance réelle sur les résultats obtenus.
La longueur d’onde 980 nm a un intérêt particulier en raison de son absorption identique dans l’eau et l’hydroxyapatite qui permet une pénétration théorique équivalente dans les tissus durs et les tissus mous.
Le Diode Epic Pro (980 nm) s’avère beaucoup trop thermique dans nos tests cliniques et peu réglable avec précision. Nous ne pouvons l’utiliser dans notre protocole, dans l’objectif de conservation des tissus sains.
Le Diode Wiser Icone (980 nm) est facilement réglable en microsecondes avec un choix des temps de pulse et des temps de repos qui permet de très hautes fréquences sans effet thermique important. Il sera retenu pour les tests de décontamination.
Le laser Diode EPIC X (940 nm) est également peu réglable avec simplement 4 modes pulsés et aucune possibilité pour l’opérateur de choisir avec précision les temps de pulse et les temps de repos. Son action thermique est également importante, nous ne pouvons donc pas utiliser ce laser directement sur les tissus osseux avec sécurité.
Le laser Diode Sirolase Blue nous intéresse en raison de sa double longueur d’onde mais la majorité des réglages proposés est bloquée dans la machine et il n’y a pas de possibilité pour l’opérateur de modifier et choisir avec précision les temps de pulse et les temps de repos.
Les effets thermiques associes avec ce rayonnement laser sont également importants, nous ne pouvons pas l’utiliser en sécurité dans le contexte envisagé de décontamination des volumes osseux.
Le laser Piion (470 + 980 nm) est proposé avec une double longueur d’onde, en laissant le choix à l’opérateur d’une seule des deux longueurs d’onde ou des deux conjointement et chaque fois une possibilité de régler les temps de pulse et les temps de repos avec une grande précision en microsecondes ou en millisecondes. Il sera donc également retenu pour les tests de décontamination.
En conclusion, le réglage précis en microsecondes et la maitrise des effets thermiques associés est plus facilement réalisable sur les lasers Diodes Wiser Icône et sur le Diode bi longueur d’onde Piion.
Nous choisissons donc ces deux lasers pour tester les longueurs d’onde de 470 nm, de 980 nm et les deux longueurs d’onde associées. Des réglages identiques permettent de comparer les effets des longueurs d’onde sélectionnées.
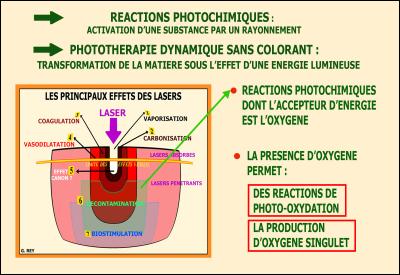
Fig. 16 – 5 lasers Diodes ont été testés cliniquement
pour permettre le choix le plus approprié aux tests envisagés
-
LES TESTS IN VITRO DE MAI 2018
Nous nous retrouvons en mai 2018 au Laboratoire du Centre Hospitalier d’Annecy en compagnie des Docteurs Pierre Bonnin et Stéphane BLAND pour tester l’effet bactéricide obtenu avec 3 longueurs d’onde différentes et 6 réglages différents (Fig. 17 et 18).
A chaque fois, 3 concentrations de bactéries différentes sont testées (102 – 104 – 106).
Nous testons successivement :
-
L’action de l’eau oxygénée seule sur la bactérie Staphylococcus Aureus
-
L’action du laser seul sur la bactérie Staphylococcus Aureus à chacune des 3 concentrations prévues
-
L’action de la « Photothérapie Dynamique sans colorant » obtenue avec l’irradiation laser après oxygénation par du Peroxyde d’hydrogène à 3 % pendant 3 minutes, sur chacune des différentes concentrations bactériennes.
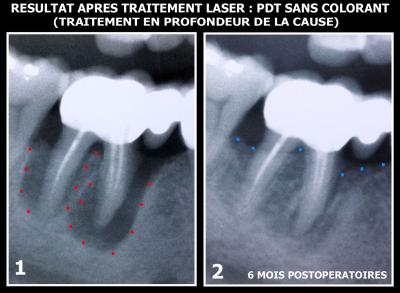
Fig. 17 et 18. – Les Docteurs Pierre BONNIN, Stéphane BLAND et Gérard REY
Au Laboratoire du Centre Hospitalier d’Annecy
Les réglages choisis pour ces premiers tests (Fig. 19)
Nous avons prévu initialement tous les réglages des lasers sélectionnés avec une puissance moyenne toujours identique de 1,2 watts, afin de tester de manière comparative les autres paramètres (longueur d’onde, … puissance de crête, …. Fréquence, …).
Avec le laser Diode Wiser Icône 980 nm, nous sélectionnons une fréquence faible de moins de 200 Hz, une fréquence moyenne de 4000 Hz et une haute fréquence de 10.000 Hz. Les puissances de crête varient de 3 à 6 watts et les Ton et Toff choisis permettent de conserver une puissance moyenne de 1,2 watts.
Avec la longueur d’onde de 470 nm (Diode Piion), nous sélectionnons une puissance de crête de 3 watts, une basse fréquence de 600 Hz et une haute fréquence de 10.000 Hz en maintenant la puissance moyenne à 1,2 watts.
Avec les deux longueurs d’onde conjointes, 980 nm + 470 nm, nous sélectionnons une puissance de crête variable de 3 à 6 watts et 3 fréquences différentes (600 Hz, 4000 Hz et 10.000 Hz) avec la même puissance moyenne que précédemment.
Deux temps d’application du rayonnement laser sont testés :
-
20 secondes : avec 2 x 10 secondes et un temps de repos intermédiaire de 10 secondes
-
40 secondes : avec 4 x 10 secondes et 3 temps de repos intermédiaire de 10 secondes.
Fig. 19 – Tableau des réglages choisis pour les tests de mai 2018

Fig. 20 – Laser Diode Wiser Icône (980 nm) avec Fig. 21 – Laser Diode Wiser Icône (980 nm) avec
réglages A3 réglages A2

Fig 22 – Laser Bi-longueur d’onde Piion (980 nm Fig. 23 – Action par va et vient de la fibre laser
+ 470 nm) avec réglages C1 dans la solution bactérienne préalablement oxygénée
Les résultats obtenus avec le Peroxyde d’Hydrogène seul, avec le laser seul et avec le laser sous eau oxygénée à 10 volumes, sont mis en culture dans des boites de Pétri afin d’analyser les éventuelles actions bactéricides obtenues au bout de quelques jours.
Fig. 24 – Mise en culture des résultats après Fig. 25 – Vérification générale de la journée de
Irradiation laser de tests
-
LES RESULTATS DES TESTS DE MAI 2018
Les premiers résultats nous parviendront au bout de 5 journées (fig. 26).
Ils permettent de constater l’inefficacité de l’eau oxygénée à 10 vol. sur le pathogène Staphylococcus Aureus.
Ils permettent de constater l’incapacité du rayonnement laser utilisé seul pour détruire cette bactérie pathogène.
Ils permettent de constater l’efficacité du protocole « Peroxyde d’Hydrogène (3 %) + laser » qui permet de détruire la bactérie Staphylococcus Aureus.
Fig. 26 – Les 1ers résultats envoyés par le Biologiste du Centre Hospitalier d’Annecy
Analyse plus précise des résultats (fi. 27)
Avec le rayonnement 980 nm, le temps d’irradiation à 40 secondes est nettement supérieur au temps d’irradiation de 20 secondes.
Deux réglages à 40 secondes (A2 et A3) obtiennent des résultats intéressants avec un meilleur résultat pour A2.
Il semble qu’à puissance moyenne égale, la fréquence soit plus importante que la puissance de crête.
Avec la longueur d’onde 470 nm, les tests confirment qu’un temps d’irradiation de 40 secondes est supérieur à un temps d’irradiation de 20 secondes et qu’une Fréquence de 10.000 Hz est nettement supérieure à une Fréquence de 600 Hz.
On constate également que la longueur d’onde de 470 nm peut également avoir un effet décontaminant intéressant.
Fig. 27 – Résultats complets de l’irradiation laser après addition
Du Peroxyde d’Hydrogène pendant 3 minutes
NOTE : Cette longueur d’onde de 470 nm a en effet une faible absorption dans l’eau, donc une bonne pénétration, mais elle est aussi immédiatement absorbée par la mélanine et l’hémoglobine de nos tissus vivants avec une augmentation de température importante (immédiatement ressentie lorsque le rayonnement impacte nos doigts, par exemple).
Cette absorption dans l’hémoglobine et la mélanine est à l’origine des qualités ablatives de ce rayonnement laser (470 nm), il convient donc de faire attention à l’échauffement des tissus voisins lors de son utilisation en décontamination ou en biostimulation. (Fig. 28)
Fig. 28 – Rappel de l’absorption des rayonnements lasers
dans les différents chromophores de nos tissus
L’utilisation d’une double longueur d’onde (470 nm + 980 nm) donne également de bons résultats bactéricides avec une fréquence de 10.000 Hz et une Puissance de Crête de 3 watts (1,5 w pour 980 nm + 1,5 w pour 470 nm).
L’irradiation pendant 40 secondes augmente l’effet bactéricide particulièrement pour les fortes concentrations.
Le réglage avec une puissance de crête de 6 watts (3 w pour 980 nm + 3 w pour 470 nm) donne un bon effet bactéricide mais engendre un effet thermique trop important, il ne sera donc pas utilisé dans les tests in vivo.
Conclusions de ces tests de mai 2018 (Fig. 29)
La PDT a un bon effet bactéricide sous Peroxyde d’Hydrogène (sans colorant) que ce soit pour les longueurs d’onde de 980 nm, de 470 nm, ou pour les deux longueurs d’onde associées conjointement.
Une fréquence de 10.000 Hz semble donner un meilleur résultat qu’une fréquence de 4000 Hz et les fréquences de quelques centaines d’Hertz ne donnent pas un résultat suffisant pour détruire Staphylococcus Aureus.
Sous réserve d’une maitrise des effets thermiques, le temps d’irradiation peut être augmenté à 40 ou 45 secondes pour un excellent effet bactéricide.
Fig. 29 – Résultats en % obtenus avec les 3 rayonnements utilisés
-
LES TESTS IN VITRO DE SEPTEMBRE 2018
Après analyse de ces 1ers résultats, il est décidé une modification des réglages en tenant compte des résultats obtenus en mai 2018, puis de tester 6 réglages différents :
-
2 avec longueur d’onde 980 nm
-
2 avec longueur d’onde 470 NM
-
2 avec la double longueur d’onde 980 nm + 470 nm.
En accord avec mon confrère le Professeur Gianluigi Caccianiga, nous décidons conjointement de tester la solution Fixlite (Peroxyde d’Hydrogène + Glycérophosphate) pour comparer son effet bactéricide par rapport au Peroxyde d’Hydrogène habituel.
Nous nous retrouvons donc au Laboratoire du Centre Hospitalier d’Annecy avec mes confrères les Dr Pierre BONNIN et Stéphane BLAND pour effectuer 3 tests, identiques avec chaque nouveau réglage, de l’effet bactéricide du protocole « PDT sans colorant » déjà testé en mai 2018. (Fig. 30)
Fig. 30 – Nouvelle journée de tests avec l’équipe du Centre Hospitalier d’Annecy
Les réglages choisis pour ces deuxièmes tests (Fig. 31)
Nous conservons une fréquence élevée et de plusieurs milliers d’Hertz variables entre 6000 et 10.000 Hz.
La puissance de crête est variable entre 2,5 et 3,5 watts.
Le temps de pulse en microsecondes est variable entre 40 s et 50 s.
Les puissances moyennes sont variables entre 0,7 w et 1,4 w.
Le temps d’irradiation du rayonnement laser est toujours identique de 45 sec. (3 X 15 secondes avec deux temps de repos de 10 secondes).
Les tests avec la solution Fixlite sont effectués dans les mêmes conditions et avec les mêmes réglages qu’avec le Peroxyde d’Hydrogène (A6 – B6 – C6).
Chaque test est effectué à 3 reprises consécutives afin de valider avec certitude l’effet bactéricide du protocole.

Fig.31 – Récapitulatif des réglages sélectionnés pour les tests de septembre 2018
NOTE : Nous avons choisi volontairement avec les 3 rayonnements lasers de sélectionner également le réglage moyen habituel utilisé pour le traitement des bactéries parodonto-pathogènes :
-
Puissance de crête : 2,5 watts
-
Ton : 50 s
-
Toff : 117 s
-
Fréquence : 6000 Hz
-
Puissance moyenne : 0,7 w
Ces indications correspondent au réglage moyen de l’effet décontaminant (Paro-Implanto) sélectionné sur l’écran du laser Diode Wiser Icône.
Ceci permettra de vérifier l’efficacité des réglages utilisés pour la destruction des bactéries parodonto-pathogènes dans les conditions cliniques des pathologies rencontrées en Odontostomatologie.
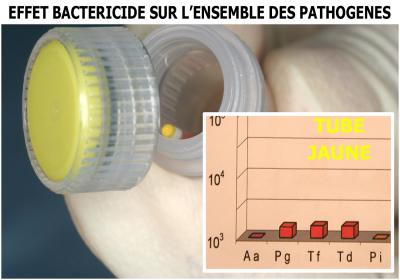
Fig. 32 – le réglage PDT moyen du Diode Wiser Icône est testé
sous Peroxyde d’Hydrogène et sous solution Fixlite
Cette journée de tests permet de choisir avec précision les paramètres de longueurs d’onde, de fréquence et de puissances (crête et moyenne) que nous utiliserons pour les tests animaliers in vivo.

Fig. 33 – Les différents rayonnements lasers sont utilisés 3 fois 15 secondes
Avec 2 repos intermédiaires de 10 secondes
-
RESULTATS DES TESTS IN VITRO DE SEPTEMBRE 2018
-
Avec la longueur d’onde de 980 nm et le réglage :
-
Pc : 2,5 w - Ton : 50 s - Toff : 117 s - 6000 Hz, correspondant au choix « PDT moyen » du Diode Wiser Icone.
Nous obtenons un bon résultat sous H2O2 10 vol. sous réserve d’une irradiation de 45 secondes (3 fois 15 secondes et 2 repos de 10 secondes) (Fig. 37).
NOTE : Le réglage à 3,5 w et 10.000 Hz donne également un bon résultat sous H2O2.
-
Avec la longueur d’onde de 470 nm et le même réglage :
-
Pc : 2,5 w - Ton : 50 s - Toff : 117 s - 6000 Hz
nous obtenons un excellent résultat sous H2O2 10 vol. ce qui démontre que les deux longueurs d’onde utilisées seules ont un potentiel bactéricide équivalent en « PDT sans colorant » (avec un léger avantage pour le rayonnement 470 nm) (voir fig. 37).
NOTE : le réglage à 10.000 Hz donne également un excellent résultat sous H2O2 (Fig. 37).
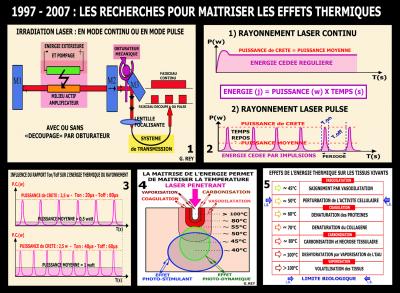
Fig. 34 – Tests de 2 longueurs d’onde différentes
-
Les tests avec la solution Flixlite s’avèrent bons avec les deux longueurs d’onde 980 nm et 470 nm pour les concentrations faibles et moyennes et moins bons pour les très fortes concentrations bactériennes de Staphylococcus Aureus (probablement plus résistante que nos pathogènes parodontaux). (Fig. 36)
-
Avec la Bi-longueur d’onde 980 nm + 470 nm et le réglage :
-
Pc : 2,5 w (980 nm : 1,3 w + 470 nm : 1,2 w) - Ton : 50 s - Toff : 117 s - 6000Hz
Nous obtenons un excellent résultat sous H2O2 10 vol. et également avec la solution Fixlite quel que soit la concentration bactérienne (Fig. 36 et 37)
Le réglage à 3,7 w et 10.000 Hz donne le même résultat excellent avec 100 % de disparition des bactéries pathogènes Staphylococcus Aureus.

Fig. 35 – Test comparatif d’une double longueur d’onde (980 nm + 470 nm)
NOTE : La reproductivité de tous ces résultats a été vérifiée par 3 essais différents effectués dans les mêmes conditions (Fig. 36 et 37).
-
Analyse comparative de l’ensemble des résultats
-
Le Peroxyde d’Hydrogène à 3 % et le rayonnement laser utilisé seul n’ont pas d’effet bactéricide sur Staphylococcus Aureus (Fig. 26 du test de Mai 2018)
-
Le rayonnement laser utilisé sous Peroxyde d’Hydrogène à 3 % avec une fréquence élevée supérieure à 5000 Hz et une puissance de crête égale ou supérieure à 2,5 w, a un effet bactéricide sur Staphylococcus Aureus avec les longueurs d’onde 470 nm et 980 nm ou avec les deux longueurs d’onde associées.
-
La maitrise des effets thermiques obtenue avec une puissance moyenne limitée entre 0,7 w et 1,4 w permet de longues irradiations (supérieures à 40 secondes) favorables à un meilleur effet bactéricide.
-
La double longueur d’onde (980 nm + 470 nm) a permis de valoriser les résultats obtenus (particulièrement avec la solution Fixlite peu efficace avec les longueurs d’onde séparées).
Pour les bactéries très résistantes, elle peut donc représenter un avantage par une amélioration de l’effet bactéricide obtenu dans le protocole de « Photothérapie Dynamique sans colorant » sous Peroxyde d’Hydrogène (Fig. 36).
-
Ce principe sera donc retenu pour les prochains tests in vivo sur les ostéonécroses liées à Staphylococcus Aureus avec le réglage suivant :
-
Pc = 3 w (980 nm 1,5 w + 470 nm 1,5 w) - Ton : 40 s - Toff : 85 s - 8000 Hz
Puissance Moyenne : 0,96 w, qui permet de limiter les effets thermiques grâce à une puissance moyenne inférieure à 1 w en conservant une haute fréquence de 8000 Hz.


Fig. 36 – Résultats comparatifs H2O2 et Fig. 37 – Résultats avec utilisation du Peroxyde
Solution Fixlite d’Hydrogène à 3 %
-
CONCLUSIONS GENERALES
-
Ces deux tests in vitro effectués au Laboratoire du Centre Hospitalier d’Annecy confirment totalement la crédibilité du protocole laser assisté utilisé sous Peroxyde d’Hydrogène dans le traitement des infections parodontales et péri-implantaires.
-
La longueur d’onde de 980 nm et les réglages :
-
Pc : 2,5 w - Ton : 50 s - Toff : 117 s - 6000 Hz
sont efficaces en décontamination dans le protocole de « PDT sans colorant » utilisé en Odontostomatologie.
-
L’amélioration du protocole pourra porter sur une irradiation plus longue avec des temps de repos intermédiaires pour une bonne relaxation thermique.
-
La double longueur d’onde peut avoir un intérêt pour les bactéries très résistantes et les concentrations bactériennes très importantes, mais le plus important reste la précision d’un réglage adapté aux pathologies et aux tissus cibles qui sont très variables en fonction des cas cliniques. Les possibilités de précision dans le choix de la puissance, de la fréquence et des temps de pulse doivent être facilement disponibles pour une utilisation clinique efficace et responsable.
Un choix final que seul le praticien peut décider après les études cliniques, radiographiques et bactériologiques effectuées pour chaque patient.
Fig. 38 – Avec des réglages appropriés, l’ensemble des longueurs d’onde testées a été efficace
BIBLIOGRAPHIE
-
ANDO Y, AOKI A, WATANABE H, ISHIKAWA I. Bactericidal effect of Erbium YAG laser on periodonto pathic bacteria. Department of Periodontology Tokyo 1996
-
CACCIANIGA GL, URSO E, MONGUZZI R, GALLO K, REY G. Effecto bactéricida del laser de diodo en periodoncia. Avances en periodoncia e implantologia oral. Dec 2007 ; vol.19 N°3
-
CHAVOIN JP, BRUNETAUD JM, GAILLOT-MAUGIN J, GODARD B, LECARPENTIER Y, LAFITTE F, MORDON S, ROUX FX, SULTAN R. Encyclopédie des lasers en médecine et en chirurgie. Ed. Piccin 1995.
-
MORITZ A, GUTNETCHT N, SCHOOP U, GOBARKHAY K, DOERBUDAK O, SPEER W. Irradiation of infected root canals with a diode laser in vivo : results of microbiological examinations lasers in surgery and medecine. 1997 ; 221-226.
-
REY G, MISSIKA P. Les lasers et la Chirurgie Dentaire. Ed. CdP Coll JPIO 2010
-
REY G, MISSIKA P. Traitements Parodontaux et Lasers. Elsevier Masson
-
REY G. L’apport du laser dans le traitement des poches parodontales. Implantodontie 2° trim. 2000 ; n°38 : 27-34
-
REY G. Efficacité des lasers en Parodontologie. La Lettre de la Stomatologie sept. 2009 ; n°43 : 5-23. Nov.2009 ; n°44 : 12-21
-
REY G. Traitement parodontal assisté aux Lasers Diodes. La Lettre de la Stomatologie Nov. 2016 ; n°72 : Spécial ADF
-
REY G. « Lasers et PDT sans colorant » - Une alternative de soins et de prévention d’intérêt collectif – L.S. nov 2017 ; N°Spécial ADF : 6-33
-
TSENG P, GILKESON CF, PALMER J, LIEW V. The bactericidal effect of a Nd Yag laser in vitro. J Dent Res 1991 ; 70 (spec. Issue) : 650 (abstr. 7)